|
|
Окислительно-восстановительные системы. Окислительно-восстановительные электроды (редокс-потенциалы). Методы измерения ЭДС. Термодинамика гальванического элемента.В 1913 году Л.В. Писаржевский выступил с электронной теорией окислительно-восстановительных процессов. Этот тип реакций осуществляется за счет перераспределения электронной плотности между атомами реагирующих веществ (переходом электронов), что проявляется в изменении степени окисления. Реакции, в результате которых изменяются степени окисления атомов, входящих в состав реагирующих веществ вследствие переноса электрона между ними, называются окислительно-восстановительными реакциями. Окислительно-восстановительный процесс состоит из 2 элементарных актов или полуреакций: окисления и восстановления. Окисление - это процесс потери (отдачи) электронов атомом, молекулой или ионом. При окислении степень окисления частиц повышается: Sn2+ - 2ē = Sn4+ Частица, отдающая электроны, называется восстановителем. Продукт окисления восстановителя называется его окисленной формой: Sn2+ (восстановитель) - 2ē = Sn4+ (окисленная форма) Восстановление - это процесс присоединения электронов частицей. При восстановлении степень окисления понижается: Fe3+ + ē = Fe2+ Частица (атомы, молекулы или ионы), присоединяющая электроны, называется окислителем. Продукт восстановления окислителя называется его восстановленной формой: Fe3+ (окислитель) + ē = Fe2+ (восстановленная форма) Окисление всегда сопровождается восстановлением, и, наоборот, восстановление связано с окислением. Окислительно-восстановительные электроды (редокси электроды). Это такие электроды, металл которых не принимает участия в электродной реакции, а лишь посредничает в передаче электронов от окислителя к восстановителю, находящихся в одном растворе. Примером такого электрода служит платина, опущенная в раствор, содержащий окисленную и восстановленную формы металла. При сочетании такого электрода с другими происходит окисление Fe3+ в Fe2+ или восстановление Fe3+ в Fe2+. Отличие редокси электрода от других типов электродов заключается в том, что продукты окисления и восстановления остаются в растворе, а металл обменивается с компонентами раствора электронами. Электродный потенциал электрода Fe2+,Fe3+|Pt. ϕ Fe2+,Fe3+|Pt = ϕ0 Fe2+,Fe3+|Pt + (RT/zF)ln(aFe3+/aFe2+) Активности компонентов в растворе. Коэффициенты активности. Растворы электролитов. Степень диссоциации. Сильные и слабые электролиты. Константа диссоциации слабого электролита. Закон разведения Оствальда. Изотонические коэффициенты. Активность компонентов раствора - это концентрация компонентов, рассчитанная с учетом их взаимодействия в растворе. Термин «активность» был предложен в 1907 году американским ученым Льюисом в качестве величины, использование которой поможет сравнительно просто описать свойства реальных растворов. Активность компонента в реальном растворе с мольной долей xi может быть определена на основе измерений парциального давления пара компонента над раствором и давления насыщенного пара над чистым веществом при заданной температуре. В общем случае активность компонента является функцией температуры, давления и мольной доли (состава). Активность компонента – это такая концентрация данного компонента в идеальном растворе, при которой он имеет такой же химический потенциал, что и в реальном растворе. Активность – не раскрывает причин отклонения данного раствора от идеального поведения, но упрощает формальное математическое описание термодинамически неидеальных растворов.
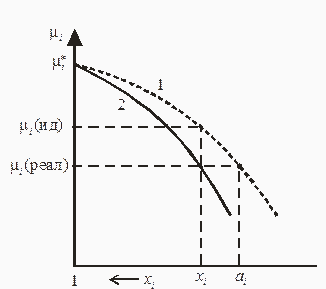
Зависимость химического потенциала компонента от концентрации в идеальном (кривая 1) и реальном (кривая 2) растворе. Коэффициент активности используется для характеристики степени отклонения реального раствора от идеального. γi = ai/xi ai = γixi Поскольку химический потенциал i-го компонента в идеальном и реальном растворах определяется выражениями μi (ид) = μi* (ж) + RT ln xi μi (реал) = μi* (ж) + RT ln ai Изменение при переходе от идеального к реальному раствору равно ∆μi = μi (реал) - μi (ид) = RT ln (ai/xi) = RT ln γi Коэффициент активности является функцией не только температуры и давления, но и концентрации. Поэтому при определении активности и коэффициента активности компонентов реальных растворов существенным является выбор стандартного состояния. В общем случае для компонентов реальных растворов (жидких и твердых тел) справедливо следующее выражение: μi = μi* (P,T) + RT ln ai = μi* (P,T) + RT ln (yixi) Чтобы полностью определить коэффициент активности, необходимо указать условия, при которых он становится равным единице. Степень диссоциации (a) - отношение числа распавшихся на ионы молекул (n) к общему числу растворенных молекул (N). Выражается в долях единицы или в %. a = n / N Различают сильные и слабые электролиты. Сильные электролиты в растворах практически диссоциированы полностью. К этой группе электролитов относится большинство солей, щелочей и сильных кислот. К слабым электролитам принадлежат слабые кислоты и слабые основания и некоторые соли: хлорид ртути (II), цианид ртути (II), роданид железа (III), иодид кадмия. Растворы сильных электролитов при больших концентрациях обладают значительной электропроводностью, причем она с разбавлением растворов возрастает незначительно. Растворы слабых электролитов при больших концентрациях отличаются незначительной электропроводностью, сильно увеличивающейся при разбавлении растворов. Изотонический коэффициент (фактор Вант-Гоффа; обозначается i) — безразмерный параметр, характеризующий поведение вещества в растворе. Он численно равен отношению значения некоторого коллигативного свойства раствора данного вещества и значения того же коллигативного свойства неэлектролита той же концентрации при неизменных прочих параметрах системы:
solut. — данный раствор, nel. solut. — раствор неэлектролита той же концентрации, Tbp — температура кипения, Tmp — температура плавления (замерзания). Закон разбавления Оствальда выведен В.Оствальдом в 1888 году и им же подтвержден опытным путём. Экспериментальное установление правильности закона разбавления Оствальда имело большое значение для обоснования теории электролитической диссоциации. Кдис = aдис2 См Это выражение носит название закона разбавления Оствальда и определяет зависимость aдис от концентрации слабого электролита в растворе: aдис = (Кдис / См(HAn))1/2. При уменьшении концентрации слабого электролита в растворе, степень диссоциации его увеличивается. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|