
|
|
Основные термодинамические закономерности идеально газовых реакцийС учетом того, что
или
где отношение под знаком логарифма – мольные доли в исходном состоянии (уравнение (17)) и состоянии равновесия. Уравнения (18), (19) имеют глубокий, но в чем-то неочевидный смысл. Чтобы несколько упростить его выявление, примем, что реакция (1) проходит при Р = 1 атм, что позволяет исключить влияние этого фактора на количество веществ А, В, С, D в состоянии равновесия. В исходном состоянии состав реакционной системы, определяющий мольные доли в неравенстве (17), был произвольным:
также является постоянной при данном значении Т. Это постоянство сохраняется и при умножении отношения равновесных мольных долей на сомножитель
следует, что само отношение под знаком логарифма также постоянная величина. Она обозначается Kp и называется константой химического равновесия идеально газовых реакций. Таким образом (опуская знак равенства)
С учетом этого, имея в виду уравнения (18), (19)
или
Выражение для константы равновесия (22) можно представить и в более краткой форме
где Рi – парциальные давления в состоянии равновесия. Подчеркнем еще раз, что термин «константа равновесия» отражает независимость отношений (22) и (25) от состава равновесной смеси, состав которой в свою очередь определяется составом смеси в исходном состоянии. Попытаемся это важное положение пояснить на примере реакции 2SО2 (г) + О2 (г) = 2SO3 (г) (26) Примем, что Т = 950К и Р = 1атм. Пусть в исходном состоянии находится следующее количество (в молях) веществ Вариант А: Вариант В: Обозначим через m* количество молей SO3, которое образовалось к моменту наступления равновесия. Тогда количество SO2, которое используется на образование
что для данного варианта очевидно. Для O2 аналогичным образом находим** y = ½ m В состоянии равновесия (вариант А) имеем
Вариант В:
Ясно, что из одного моля SO2 и одного моля O2 образуется меньше SO3, чем из двух молей SO2. Даже при полном превращении SO2 в SO3 в первом случае может образоваться лишь 1 моль, во втором – 2 моля. _______________________ * от лат. «moles» – масса **При стехиометрическом уравнении аА + вВ → сС + dD обозначая количество молей С в состоянии равновесия через m находим: а – с yа – m y = Аналогично для В и D находим yВ = Итак, m2(В) > m1(А) тогда 1 – m1 ≠ 2 – m2; 1 – m1 ≠ 1 – m2 m1 ≠ m2 Общее число молей в состоянии равновесия А: B: Мольные доли: А: В: Количество молей и мольные доли в состояниях равновесия, обозначенных А и В различны, но из уравнения (19) следует, что
Для реакции (25)(958К) = −14,6 кДж тогда
4. Видоизмененные выражения Кр В уравнении (22) отношение мольных долей обозначают Кх. Тогда
Например, такой особенностью обладает реакция H2 (г) + Br2 (г) → 2HBr, В этом случае постоянном остается не только отношение парциальных давлений, но и мольных долей. Более того при ∆ν = 0 является постоянным и отношение количества молей в состоянии равновесия. Запишем (22) в таком виде
но ∆ν=0 и (c + d) = (a + b) Таким образом, если ∆ν = 0
Для такого рода реакций Кр, Кх и Кn выражаются через отношение количества молей в состоянии равновесия. Из уравнения (24) следует еще одна важная особенность константы равновесия Имея в виду (27) можно написать
Но чтобы при возрастании давления
При увеличении давления дробь уменьшается и И наконец, при ∆ν=0
что означает, что давление в этом случае не оказывает влияния на состав равновесной смеси. 5. Определение Кр расчетным методом 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 неравенство (4) уравнения (5), (6), (7) приобретают вид
неравенство (4) уравнения (5), (6), (7) приобретают вид


 ,
,  ,
,  ,
,  . В процессе реакции по мере продвижения к состоянию равновесия уменьшается количество реагентов и увеличивается количество продуктов. Эти изменения связаны стехиометрическим уравнением (1), которое справедливо для любого состава исходной смеси. По этой причине количество веществ nA, nB, nC, nD и соответствующие мольные доли в состоянии равновесия будут зависеть от состава исходной смеси: каждому индивидуальному составу исходной смеси соответствует индивидуальный состав веществ при равновесии. Но поскольку
. В процессе реакции по мере продвижения к состоянию равновесия уменьшается количество реагентов и увеличивается количество продуктов. Эти изменения связаны стехиометрическим уравнением (1), которое справедливо для любого состава исходной смеси. По этой причине количество веществ nA, nB, nC, nD и соответствующие мольные доли в состоянии равновесия будут зависеть от состава исходной смеси: каждому индивидуальному составу исходной смеси соответствует индивидуальный состав веществ при равновесии. Но поскольку  одна и та же величина при любом составе исходной и соответствующей ему равновесной смеси, величина, равная
одна и та же величина при любом составе исходной и соответствующей ему равновесной смеси, величина, равная
 , Р – произвольное давление. Из постоянства логарифма величины
, Р – произвольное давление. Из постоянства логарифма величины


 = 1;
= 1;  1;
1;  = 1
= 1 можно найти по правилу пропорциональности: в соответствие со стехиометрическим уравнением на образование 2 молей SO3 необходимо 2 моля SO2; для m молей SO3 – y молей SO2.
можно найти по правилу пропорциональности: в соответствие со стехиометрическим уравнением на образование 2 молей SO3 необходимо 2 моля SO2; для m молей SO3 – y молей SO2. ;
; 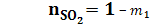 ;
; ;
;  ;
; m
m m; yD =
m; yD =  m
m

 ;
;  ;
; 
 ;
;  ;
; 




 . По определению и по физическому смыслу
. По определению и по физическому смыслу  характеризующая состояние равновесия, одна и та же величина.
характеризующая состояние равновесия, одна и та же величина. (30)
(30) в уравнении (30). Направление, в котором происходит изменение
в уравнении (30). Направление, в котором происходит изменение 
 (31)
(31)