|
|
Основы количественного анализа
Задачей аналитической химии является разработка методов определения состава различных объектов, как природного, так и искусственного происхождения. Методы химического анализа включают качественный анализ – идентификация (обнаружение) компонентов анализируемого объекта и количественный анализ – определение содержания (массы, концентрации) или количественного соотношения компонентов в анализируемом объекте. Методы количественного анализа широко применяются во всех областях деятельности человека, в том числе в биохимии и медицине, где диагностика многих заболеваний основана на сравнении результатов анализа крови, мочи, желудочного сока, спинномозговой жидкости и др., взятых у конкретного больного, с нормальным содержанием определяемых компонентов в этих биожидкостях. Количественный анализ используется также при определении качества пищевых продуктов, питьевой воды, лекарственных препаратов и др. Методы количественного анализа.Методы количественного анализа моно разделить на химические и физико-химические. Химические методы основаны на проведении химических реакций между изучаемым объектом и специально подобранным реактивом. Объектом как правило служит раствор. Определение проводится по количеству затраченного реактива или по количеству полученного продукта реакции. Различают гравиметрический и титриметрический методы анализа. Гравиметрический анализ основан на полном количественном выделении компонента раствора (как правило, в виде осадка) и последующем его взвешивании. Титриметрический анализ заключается в точном определении объема раствора реактива с известной концентрацией, необходимого для полного протекания реакции с данным объемом анализируемого раствора. Физико-химические методы анализа – это аппаратурные методы, основанные на количественном изучении зависимости «состав – физическое свойство объекта». К ним относится потенциометрия, кулонометрия, спектрофотометрия и другие. Вне зависимости от метода количественный анализ включает следующие этапы: отбор и подготовка пробы для анализа; перевод анализируемой части пробы в состояние, удобное для анализа; расчет результата единичного определения; расчет результата анализа путем усреднения результатов единичных определений. Теоретические основы титриметрического анализа.Титриметрия – совокупность методов количественного анализа, основанных на измерении количества реагента, необходимого для взаимодействия с определяемым веществом в растворе в соответствии со стехиометрией химической реакции между ними. В основе титриметрического метода анализа лежит один из законов стехиометрии – закон эквивалентов. Химическим эквивалентом называется реальная или условная частица вещества, в обменной реакции присоединяющая или замещающая один однозарядный ион (протон), а в окислительно-восстановительной реакции – участвующая в переносе одного электрона. Химический эквивалент вещества Х обозначается В обменных реакциях: Al2(SO4)3 + 3 BaCl2 → 2 AlCl3 + 3 BaSO4 H3PO4 + 2 KOH → K2HPO4 + 2 H2O эквиваленты реагирующих веществ равны:
Фактор эквивалентности Для окислительно-восстановительной реакции: 2 KMnO4 + 5 H2O2 + 3 H2SO4 → 2 MnSO4 + 5 O2 + K2SO4 + 8 H2O эквивалент перманганата калия (MnO4 - + 8Н+ + 5е- → Mn2+ + 4 H2O) равен а эквивалент пероксида водорода (H2O2 – 2е-→ O2 + 2Н+) равен
Таким образом, в реакцию вступают равные количества веществ эквовалентоа окислителя и восстановителя:
Закон эквивалентов: вещества реагируют друг с другом в равных количествах их эквивалентов. Понятие химического эквивалента значительно упрощает расчеты в количественном анализе. Молярную концентрацию и молярную массу эквивалента вещества Х можно рассчитать по формулам:
Тогда закон эквивалентов можно записать в виде:
где V(X) и V(Y) – объемы реагирующих веществ Х и Y. Эта формула позволяет рассчитать концентрацию эквивалента определяемого вещества (анализируемый раствор), если точно известна концентрация реагирующего с ним вещества (титрант). Добавление раствора титранта к анализируемому раствору небольшими порциями (по каплям) называется титрованием. При проведении титрования контролируют объем добавленного титранта. Процесс титрования заканчивается при достижении точки эквивалентности – состояния системы, в котором количества веществ эквивалентов анализируемого вещества (Х) и титранта (Т) становятся равны. Измерив объем титранта рассчитывают концентрацию эквивалента анализируемого вещества, используя (1.1):
Реакции, используемые в титриметрическом анализе, должны осуществляться достаточно быстро, быть практически необратимыми, не сопровождаться образованием побочных продуктов и позволять надежно фиксировать точку эквивалентности. В зависимости от типа химической реакции выделяют следующие методы титриметрического анализа:
По способам титрования различают: прямое титрование, когда к раствору анализируемого вещества непосредственно добавляют раствор титранта; при обратном титровании к раствору анализируемого вещества добавляют строго определенное количество вспомогательного реагента, избыток которого титруют раствором титранта; при косвенном титровании к раствору анализируемого вещества добавляют нефиксированный избыток вспомогательного реактива с последующим титрованием продукта реакции раствором титранта.
Кислотно-основные реакции в титриметрическом анализе.Определение веществ с применением в качестве титрантов стандартных растворов кислот называется ацидиметрия, а с применением растворов щелочей – алкалиметрия. Ацидиметрическим титрованием можно определить содержание в растворе сильных и слабых оснований, а также солей, образованных слабыми кислотами и гидролизующихся по аниону. Точка эквивалентности в этих случаях находится в кислой среде, в области рН≤7. Алкалиметрически можно определить содержание в растворе сильных и слабых кислот, а также солей, образованных слабыми основаниями и гидролизующихся по катиону. Точка эквивалентности в этих случаях находится в щелочной среде, в области рН ≥7. Зависимость рН (или какого-либо другого физического свойства) от объема добавленного титранта называется кривой титрования, на ней фиксируется скачок – резкое изменение свойства – в точке эквивалентности (рис.1). Точка эквивалентности определяется, как правило, визуально по изменению окраски раствора. Часто для этих целей используют кислотно-основные индикаторы – органические соединения, которые изменяют окраску в зависимости от концентрации ионов Н+, то есть от рН раствора. Изменение цвета индикатора отмечается в области рН, которая называется интервалом перехода индикатора (таблица 2 и таблица 4 приложения). Индикатор подбирают так, чтобы интервал перехода окраски включал значение рН, которое должен иметь раствор в точке эквивалентности (рис. 1). Смеси индикаторов, которые непрерывно изменяют окраску во всей области рН от 1 до 14, называются универсальными. Их используют для приблизительной оценки рН растворов. Оборудование и методика проведения титриметрического анализа.Основным оборудованием в титриметрическом анализе является мерная химическая посуда – бюретки, мерные пипетки, мерные и конические колбы (рис.2). Мерная посуда обязательно должна иметь маркировку с указанием вместимости (в мл), которая реализуется при наполнении жидкостью при указанной температуре. Бюретка представляет собой калиброванную стеклянную трубку с клапанным устройством на оттянутом конце, предназначенную для добавления растворов небольшими порциями или каплями и измерения объема. Цена бюретки вместимостью 25 мл или 50 мл составляет 0,1 мл. Заполняется бюретка раствором через верхнее отверстие с помощью воронки. Мерные пипетки – это стеклянные трубки, предназначенные для отмеривания и переноса заданного объема раствора для проведения анализа – аликвотной доли – из одного сосуда в другой. Пипетка может быть рассчитана на отмеривание одного объема (пипетка Мора) или на любой объем в пределах вместимости (градуированная пипетка). Для заполнения пипеток используют медицинские груши. Мерные колбы представляют собой плоскодонные колбы с узким горлышком, на которое нанесена кольцевая метка. Мерные колбы предназначены для приготовления растворов точно заданного объема. Конические колбы – плоскодонные колбы, предназначенные для непосредственного проведения реакций. Этапы выполнения титриметрического анализа показаны на рисунке 3. Анализируемый раствор переносят в мерную колбу (1) и добавляют дистиллированную воду строго до метки. Из мерной колбы с помощью пипетки Мора отбирают аликвотную долю анализируемого раствора (2) и переносят в коническую колбу для титрования (3). Перед началом титрования в колбу при необходимости добавляют вспомогательные растворы или индикатор. Титруют (4) анализируемый раствор в конической колбе раствором титранта из бюретки, предварительно заполнив ее до нулевой метки. Следует помнить, что заполнение бюретки и измерение объемов для неокрашенных или слабоокрашенных жидкостей проводят по центру мениска жидкости, а для интенсивноокрашенных жидкостей – по краю мениска.
Задание для самостоятельной подготовки При подготовке к занятию необходимо усвоить следующие основные понятия: 1) Количественный анализ; 2) Химический эквивалент 3) Закон эквивалентов; 4) Титрование и титрант; 5) Точка эквивалентности и кривая титрования; 6) Основные методы титриметрического анализа и способы титрования; 7) Ацидиметрия и алкалиметрия; 8) Принцип выбора индикатора; Для подготовки к занятию в качестве основного рекомендован учебник [ ], дополнительно может быть использована литература: [ ]

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 .
.
 показывает, какая часть структурной или формульной единицы вещества соответствует ее эквиваленту в данной реакции.
показывает, какая часть структурной или формульной единицы вещества соответствует ее эквиваленту в данной реакции.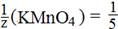



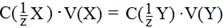 (1.1)
(1.1)