
|
|
Комплексонометрическое определениеКАФЕДРА ХИМИИ
УИРС
Тема: «Количественное определение массовой доли (W%) меди сульфата »
Выполнила: Студентка 2 курса ФФ гр. 3802 Селюнина А.В. Проверил: Белоусова Н.И.
Томск 2010 Фармакопейная характеристика препарата
Cupri sulfas Меди сульфат Cuprum sulfuricum CuSO4*5H2O Мол.масса=249,68 г/моль Описание: Синие кристаллы или синий кристаллический порошок без запаха, металлического вкуса. Медленно выветривается на воздухе. Водные растворы имеют слабокислую реакцию. Растворимость: Легко растворим в воде, очень легко – в кипящей воде, практически нерастворим в 95%-ом спирте. Подлинность: ü Раствор препарата (1:20) при соприкосновении с железом покрывает его красным налётом металлической меди. ü При добавлении по каплям к такому же количеству препарата раствора NH3 образуется голубой осадок, растворяющийся в избытке реагента. Полученный раствор имеет тёмно-синее окрашивание. ü Препарат даёт характерную реакцию на сульфаты: к 2мл р-ра сульфата (0,005-0,05 г иона SO42-) прибавляют 0,5 мл разведённой соляной кислоты и 0,5 мл р-ра барий хлорида, образуется белый осадок, нерастворимый в разведённых кислотах. Прозрачность раствора: Раствор 0,5 препарата в 10 мл воды должен быть прозрачным. Допустимые примеси: Препарат должен содержать не более 0,2% солей металлов, не осождаемых сероводородом. Хранение: Список Б. в хорошо упакованной таре. Высшая разовая доза: Внутрь 0,5г (однократно как рвотное средство). Применение: ü CuSO4*5H2O (медный купорос) применяется наружно в виде 0,25% р-ра как антисептическое и вяжущее средство при коньюктивитах. Воспалительных процессах мочеполовой системы. ü При ожогах кожи фосфором обильно смачивают обожжённый участок 5% р-ом. ü Малые дозы (5-10 капель с молоком) применяют внутрь при анемии. Большие дозы вызывают рвоту.
Йодометрическое титрование Ход работы:
1.Приготовление стандартного раствора K2Cr2O7 ( Cfэкв=0,02 моль/л, методом точной навески) 2.Приготовление раствора титранта Na2S2O3*5H2O (Cfэкв=0.02 моль/л, методом приблизительной концентрации). 3.Стандартизация раствора титранта Na2S2O3*5H20 (методом замещения) Реакции: а) K2Cr2O7 + 6KJ + 7H2SO4 → Cr2(SO4)3 + 3J2 + 4K2SO4 + 7H2O б) J2 + 2Na2S2O3 → 2NaJ + Na2S4O6
Методика: в 3 колбы для титрования берут аликвоты K2Cr2O7 (по 5 мл), добавляют 10мл KJ (W=5%), по 2 мл р-ра H2SO4 (2 моль/л). Колбы закрывают часовым стеклом. Оставляют в темноте на 5-10 мин. Выделившийся в результате реакции йод оттитровывают р-ом титранта Na2S2O3 из пипетки на 10мл до соломенно-жёлтого цвета, затем добавляют крахмал и титруют до исчезновения синей окраски. Определяют средний объём титранта и рассчитывают его концентрацию эквивалента.
С(Na2S2O3)=
V1(Na2S2O3)=6,1; V3(Na2S2O3)=6,2;
С(Na2S2O3)=
4.Определение W% CuSO4*5H2O (фармакопейная методика). Определение проводят методом замещения. Реакции: а) 2CuSO4 + 4KJ б) J2 + 2Na2S2O3 → 2NaJ + Na2S4O6
Методика: навеску препарата растворяют в 5мл дист.воды, прибавляют 0,4 мл разбавленной H2SO4, 0,3г сухого KJ; выделившийся в реакции йод титруют р-ром Na2S2O3, фиксируя конец титрования с помощью крахмала. титрование ведут 5 раз. Из каждого результата рассчитывают W% CuSO4 по формуле:
W%=
1. m(нав)1=0,101г; m(в-ва)1 = V(Na2S2O3)1= 24,5мл; W%1=
2. m(нав)2=0,099г; m(в-ва)2 = V(Na2S2O3)2= 24,3мл; W%2= 3. m(нав)3=0,096г; m(в-ва)3 = V(Na2S2O3)3= 23,4мл; W%3= 4. m(нав)4=0,098г; m(в-ва)4 = V(Na2S2O3)4= 24,2мл; W%4= 5. m(нав)5=0,104г; m(в-ва)5= V(Na2S2O3)5= 24,7мл; W%5=
Затем проводят статистическую обработку данных.
n – число измерений; Xi – результат единичного измерения;
X ±
Комплексонометрическое определение
Ход работы:
1.Приготовление стандартных MgSO4*7H2O и ZnSO4 (C=0,02 моль/л методом точной навески) 2.Приготовление раствора титранта ЭДТА (трилона Б) (С=0,02 моль/л методом приблизительной концентрации). 3.Стандартизация раствора титранта ЭДТА (основана на реакциях комплексообразования). Реакции: а) Mg2+ + HJnd2- + OH- →
б)
Методика: в 3 колбы для титрования берут аликвоты MgSO4 (по 5 мл), добавляют по 10 мл аммиачного буферного раствора (для создания среды), добавляют по 0,1 г порошка индикатора эриохрома чёрного Т, тщательно перемешивают. Пипетку на 10 мл заполняют раствором титранта ЭДТА и титруют содержимое колб по очереди до перехода окраски из вишнёво-красной в синюю (цвет свободного индикатора). Определяют средний объём титранта и рассчитывают его концентрацию.
С(ЭДТА)=
V1(ЭДТА)=5,2; V3(ЭДТА)=5,2;
С(ЭДТА)=
4. Определение W% CuSO4*5H2O. Определение проводят методом обратного титрования. Реакции: а) Cu2+ + б) в) Zn2+ +
Методика: навеску препарата растворяют в дист.воде в мерной колбе на 50 мл. в 3 колбы для титрования берут аликвоты (по 2 мл) полученного раствора, добавляют точно измеренный избыточный объём титранта ЭДТА (по 6 мл), нагревают для ускорения реакции. Затем к охлаждённому р-ру добавляют аммиачный буферный раствор (6 мл) и индикатор эриохром чёрный Т, тщательно перемешивают. Затем избыточное количество титранта ЭДТА оттитровывают с помощью стандартизированного р-ра ZnSO4. Точку конца титрования фиксируют по переходу окраски из синей в вишнёво-красную. Из каждого результата рассчитывают m в-ва CuSO4, данные усредняют и рассчитывают W% по формуле:
W%=
mв-ва =
Затем проводят статистическую обработку данных. (пояснения к обозначениям см.выше)

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 , моль/л
, моль/л
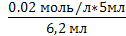 = 0,0161 моль/л
= 0,0161 моль/л 2CuJ2 + J2 + 2K2SO4
2CuJ2 + J2 + 2K2SO4 , а mв-ва =
, а mв-ва = 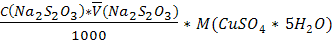 .
. =0,09848
=0,09848 = 97,5%
= 97,5% =0,09768
=0,09768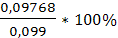 = 98,6%
= 98,6%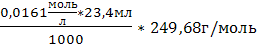 =0,09406
=0,09406 = 97,9%
= 97,9% =0,09728
=0,09728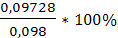 = 99,2%
= 99,2% =0,09929
=0,09929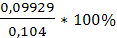 = 95,4%
= 95,4% – результат среднего значения измеренной величины;
– результат среднего значения измеренной величины; – разность значения единичного и среднего измерений;
– разность значения единичного и среднего измерений; – квадрат разности;
– квадрат разности;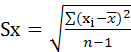 – стандартное отклонение единичного измерения;
– стандартное отклонение единичного измерения; или
или  =
=  - стандартное отклонение
- стандартное отклонение  ;
; – границы доверительного интервала,
– границы доверительного интервала, 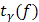 – коэф-т Стьюдента.
– коэф-т Стьюдента. – результат анализа.
– результат анализа.
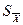
 + H2O;
+ H2O;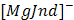 + H2Y2- + OH- →
+ H2Y2- + OH- →  +
+  + H2O.
+ H2O.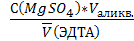 , моль/л
, моль/л
 0,01912 моль/л
0,01912 моль/л + 2OH- →
+ 2OH- →  + 2H2O;
+ 2H2O;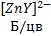 + 2H2O;
+ 2H2O; + H2O;
+ H2O;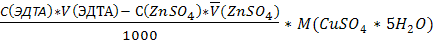 *
*  ,г
,г ср
ср