|
|
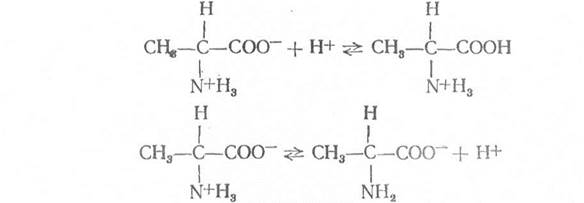
Метод распределительной (радиальной) хроматографии на бумагеМетоды выделения и количественного определения аминокислот 1. Амфотерные свойства α-аланина Принцип реакции. Алании в водном растворе существует в форме биполярного иона и обладает кислотными и основными свойствами.
Материалы и реактивы. Водный 1 %-ный раствор α-аланина, 0,1 %-ный раствор соляной кислоты, подкрашенный индикатором конго в синий цвет (кислая среда), 0,1 %-ный раствор гидроксида натрия, подкрашенный фенолфталеином в розовый цвет (щелочная среда). Оборудование. Стеклянные палочки, пробирки со штативом, пипетки градуировочные, капельницы. Ход работы. В 2 пробирки вносят по 5 капель раствора α -аланина. В одну из них добавляют, перемешивая, по каплям раствор соляной кислоты до появления розово-красной окраски (щелочная среда). В другую пробирку, постоянно перемешивая, вливают по каплям раствор гидроксида натрия до исчезновения окраски (кислая среда).
Выделение свободных аминокислот из биологического материала Принцип метода. Свободные аминокислоты извлекают из биологического материала 75—80 %-ным водным раствором этанола. Аминокислоты в вытяжке из биологического материала обнаруживают реакцией с нингидрином. Материалы и реактивы. Сухой размолотый биологический материал (ткань экспериментального животного, фиксированная этанолом при нагревании и переведенная в сухой порошок), складчатые фильтры бумажные, 70 %-ный водный раствор этилового спирта, 1 %-ный водный раствор соляной кислоты, 1 %-ный раствор нингидрина в 95 %-ном ацетоне. Оборудование. Стеклянные палочки, пробирки, капельницы, пипетки, ступка фарфоровая с пестиком, чашка выпаривательная, водяная баня, термометр лабораторный, воронки стеклянные, часы. Ход работы. В ступку помещают 2 г размолотого сухого биологического материала и заливают 10 мл 75 %-ного раствора этилового спирта, нагретого до t 60—70 °С на водяной бане. Полученную смесь тщательно растирают в течение 15 мин и фильтруют через вставленный в воронку складчатый бумажный фильтр в чашку для выпаривания, используя ее в качестве приемника. Чашку помещают на кипящую водяную баню и полностью выпаривают спирт. Полученный сухой остаток растворяют в 1 мл раствора соляной кислоты и тщательно его растирают стеклянной палочкой в течение 10-15 мин. Для обнаружения аминокислот в вытяжке к 5 каплям смеси добавляют 2 мл дистиллированной воды (разводят вытяжку) и 3-4 капли раствора нингидрина. Полученную смесь тщательно перемешивают и нагревают на водяной бане при t 70 °С в течение 5 мин. Появляется сине-фиолетовая окраска, свидетельствующая о наличии в пробе α-аминокислот. Если плотность окраски вытяжки с нингидрином измерить с помощью колориметра и сопоставить с плотностью окраски нингидрином смеси α-аминокислот известной концентрации, то можно рассчитать концентрацию α -аминокислот в исследуемой пробе.
Определение отдельных аминокислот хроматографическими методами Метод распределительной (радиальной) хроматографии на бумаге Принцип метода. Применение метода распределительной хроматографии на бумаге для разделения аминокислот основано на различии в коэффициентах распределения отдельных аминокислот между двумя несмешивающимися жидкостями. Используемая в качестве инертного носителя хроматографическая бумага способна удержать в порах большое количество неподвижной жидкой фазы. Коэффициент распределения Rf, определяемый как отношение расстояний, пройденных аминокислотой и подвижной фазой от точки старта, является характерной величиной для каждой аминокислоты в определенных условиях опыта (состав растворителя, температура, сорт хроматографической бумаги). Положение аминокислот на бумаге определяют с помощью цветной реакции с нингидрином. В присутствии нингидрина отдельные аминокислоты выявляются в виде пятен, окрашенных в голубой, фиолетовый, желтый или другой цвет (в зависимости от химической структуры аминокислоты). Идентификацию аминокислот в смеси проводят по распределению известных аминокислот (стандартов). Материалы и методы. Хроматографическая бумага, растворитель – смесь н-бутанола, уксусной кислоты, воды (4:1:1), смесь аминокислот и их стандартные растворы (0,1 %-ный растворы аланина, лейцина и глутаминовой кислоты), свежеприготовленный нингидриновый реактив (95 мл 0,5 %-ного раствора нингидрина в 95 %-ном ацетоне, 1 мл ледяной уксусной кислоты и 4 мл дистиллированной воды). Оборудование. Эксикатор или чашка Петри, пульверизатор, микропипетки, сушильный шкаф, карандаш, линейка, часы. Ход работы. Хроматографическую бумагу вырезают в форме круга, диаметр которого равен поверхностному радиусу эксикатора (или чашки Петри). Простым карандашом круг разделяют на сегменты, в центре делают небольшое отверстие (0,5—1 см), в которое вставляют свернутую в трубочку фильтровальную бумагу (фитиль). Изменяя толщину и длину фитиля, который опущен в растворитель, регулируют скорость подачи растворителя на хроматографическую бумагу. Карандашом у основания фитиля на хроматографической бумаге в каждом сегменте намечают точку нанесения аминокислот. На один из сегментов с помощью микропипетки наносят смесь аминокислот (5-10 мкл раствора аланина, лейцина и глутаминовой кислоты), на другой сегмент – такое же количество аминокислот стандартов. Затем хроматографическую бумагу высушивают на воздухе в течение 10 мин. В эксикатор (или чашку Петри) наливают растворитель – смесь н-бутанола, уксусной кислоты и воды (4:1:1) в таком объеме, чтобы фитиль был погружен в растворитель. Круговую хроматограмму помещают в эксикатор (или между двумя половинками чашки Петри). Хроматограмма с диаметром 12 см образуется примерно через 1 ч, с диаметром 20 см – через 2 ч. После завершения распределения (фронт растворителя дошел до установленной отметки) хроматограмму высушивают и проявляют, опрыскивая нингидриновым реактивом из пульверизатора и прогревая в сушильном шкафу в течение 10 мин при температуре 110 оС Сравнивая положение пятен смеси аминокислот с положением пятен аминокислот-стандартов, проводят идентификацию пятен смеси аминокислот. С помощью линейки определяют расстояния, пройденные фронтом растворителя и аминокислотами, и вычисляют значения коэффициента распределения.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|