
|
|
Особенности строения и химические свойства.12 6.1. Свойства аминов как оснований (акцепторов протонов)
Связь протона с амином, как и с аммиаком, образуется по донорно-акцепторному механизму за счет неподеленной электронной пары атома азота. 2. Взаимодействуя с кислотами, амины образуют соли:
Соли аминов – твердые вещества, хорошо растворимые в воде. При нагревании щелочи вытесняют из них амины:
Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его p-электронами.
Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, H2SO4), а его водный раствор не окрашивает лакмус в синий цвет. Таким образом, основные свойства (в газовой фазе) изменяются в ряду: C6H5NH2 < NH3 < RNH2 < R2NH < R3N 6.2. Взаимодействие с азотистой кислотой.Азотистая кислота HNO2 – неустойчивое соединение. Поэтому она используется только в момент выделения. Образуется HNO2, как все слабые кислоты, действием на ее соль (нитрит) сильной кислотой: KNO2 + HCl à НNO2 + KCl или NO2 + H à НNO2 Строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различения первичных, вторичных и третичных аминов. Первичные алифатические амины c HNO2 образуют спирты:
R-NH2 + HNO2 à R-OH + N2 + H2O
Первичные ароматические амины при повышенной температуре реагируют аналогично, образуя фенолы. Вторичные амины (алифатические и ароматические) под действием HNO2 превращаются в нитрозосоединения (вещества с характерным запахом):
R2NH + H-O-N=O à R2N-N=O + H2O Реакция с третичными аминами приводит к образованию неустойчивых солей и не имеет практического значения. 6.3. Окисление аминов. Амины, особенно ароматические, легко окисляются на воздухе. В отличие от аммиака, они способны воспламеняться от открытого пламени. 4СH3NH2 + 9O2 à 4CO2 + 10H2O + 2N2 6.4. Образование N-замещенных амидов кислот (ациламинов). Действием на первичные и вторичные амины галоидангидридов или ангидридов кислот можно заменить связанный с азотом атом водорода на кислотный радикал, причем получаются замещенные амиды органических кислот: CH3CO-Cl + H2N-R à CH3CO-NHR + HCl (CH3CO)2O + NH(CH3)2 à CH3CO-N(CH3)2 + CH3COOH Третичные амины, не имеющие при атоме азота атом водорода, с галоидангидридами и ангидридами кислот не реагируют. 6.5. Действие галоидов. Действием хлора или брома в присутствии щелочи на первичные или вторичные амины можно заменить на галоид атомы водорода в аминогруппе и получить галоидамины: CH3NH2 + 2Br2 à CH3NBr2 + 2HBr (CH3)2NH + Br2 à (CH3)2NBr + HBr
Бромамины – легко разлагающиеся вещества, с резким запахом. Взаимодействуют с водой с образованием аминов и бромноватистой кислоты. 6.6. Образование изонитрилов. Действием на первичные амины хлороформа в присутствии спиртовой щелочи получают изонитрилы:
RNH2 + CHCl3 à R-N=C + 3HCl 6.7. Взаимодействие с галогенпроизводными. Амины присоединяют галогеналканы RCl, с образованием донорно-акцепторной связи N-R, которая также эквивалентна уже имеющимся. 6.8. Конденсация с альдегидами и кетонами. Конденсация первичных аминов с альдегидами и кетонами приводит к образованию иминов или так называемых оснований Шиффа, соединений, содержащих фрагмент -N=C<: R-NH2 + O=CHR’ à R-N=CH-R’ + H2O R-NH2 + O=CR’R” à R-N=CR’R” + H2O
Реакция обратимая и экзотермическая, приводит к образованию иминов, или азометинов, или оснований Шиффа, в честь открывшего эти соединения. Имины широко используются в фармацевтической промышленности. Они служат исходным сырьем для производства ценных лекарственных препаратов: антибиотиков, противоаллергических, противовоспалительных и противоопухолевых средств. Их применяют также в качестве ингредиентов резиновых смесей и ингибиторов кислотной коррозии.
7. Экспериментальная часть.
Опыт № 1. Получение сернистой соли анилина. К 0,5 мл анилина добавить несколько капель разбавленной серной кислоты, при этом выделяется в виде белых кристаллов сернистая соль анилина. Напишите уравнение реакции. Опыт №2. Реакция анилина с ангидридами кислот. Получение ацетанилина. Смесь 1 мл анилина и 2 мл воды помещают в пробирку, энергично взбалтывают и добавляют 1 мл уксусного ангидрида. Закрывают пробирку пробкой, снова сильно встряхивают её содержимое. Смесь разогревается и затем затвердевает. Напишите уравнение реакции. Опыт №3. Конденсация анилина с мочевиной. В пробирку помещают 0,3 г мочевины и 1 г анилина. Нагревают смесь на пламени горелки при частом взбалтывании. От начала выделения пузырьков газа продолжают нагревать ещё 6 минут. При реакции конденсации образуется две несмешивающиеся жидкости, затем, после обильного выделения аммиака, смесь загустевает и становится однородной. При охлаждении к затвердевшему продукту реакции добавляют 5 мл раствора соляной кислоты и нагревают смесь до полного растворения непрореагировавших исходных веществ. Образовавшаяся дифенилмочевина остается в осадке, её отделяют на воронке Бюхнера и сушат на воздухе. Напишите уравнение реакции. Опыт №4. Конденсация анилина с бензальдегидом. Конденсация аминов с альдегидами и кетонами приводит к образованию иминов или оснований Шиффа - соединений, содержащих фрагмент -N=C<. Слейте в пробирке 1 мл анилина и 1,1 мл бензальдегида. Обратите внимание на экзотермический эффект реакции. Осторожно нагрейте над пламенем горелки. Обратите внимание на выделяющуюся воду. После охлаждения образовавшийся имин кристаллизуется. Напишите уравнение реакции. Опыт №5. Диазотирование ароматических аминов. Первичные ароматические амины при взаимодействии с азотистой кислотой образуют непрочные диазосоединения, выделяя при этом воду. В колбу помещают 10 мл разбавленной соляной кислоты и растворяют в ней 1 мл анилина. После охлаждения к раствору медленно и постепенно добавляют 0,5 г азотистого натрия, растворенного в 5 мл воды (процесс диазотирования). При этом смесь не должна разогреваться, в противном случае ее охлаждают на водяной бане в воде со льдом. При выделении пузырьков газа прибавление нитрита натрия замедляют. Через 5-10 минут после окончания добавления нитрита полученный раствор проверяют на предмет окончания реакции диазотирования. (Содержимое колбы оставить для следующего опыта). Напишите уравнение реакции. Опыт №6. Исследование свойств полученных диазосоединений. а) Разложение диазобензола (хлористого фенилдиазония). В пробирку помещают 1-2 мл полученного в предыдущем опыте раствора диазобензола и нагревают его на небольшом пламени спиртовки. Диазобензол разлагается с выделением пузырьков азота. При этом появляется характерный запах фенола. Напишите уравнение реакции б) Реакция образования азосоединения (получение бензолазонафтола). Полоску льняной ткани, предварительно смоченную дистиллированной водой и диазобензолом (полученным в опыте №4), опустите в стаканчик с 3 мл щелочного раствора α- или β-нафтола. Перемешайте стеклянной палочкой. Ткань окрашивается в красный цвет. Напишите уравнение реакции.
Техника безопасности
1. Работу с уксусным ангидридом проводить только в вытяжном шкафу и под наблюдением преподавателя. 2. Нагревание пробирок с растворами производить в вытяжном шкафу, равномерно нагревая нижнюю часть пробирки, в которой находятся жидкости. Отверстие пробирки должно быть направлено от себя и окружающих. 3. При работе пользоваться только хорошо высушенными пробирками.
Контрольные вопросы
1. Напишите структурные формулы трех изомеров толуидина, назовите их по международной и рациональной номенклатуре. 2. Выбрать из предложенных соединений первичные, вторичные, третичные амины. Дайте название всем соединениям. 3. Как с помощью реакции Н.И.Зимина получить анилин? 4. Как получить из бромбензола п-броманилин? 5. Какая реакция аминов является качественной реакцией на амино-группу?
Список рекомендуемой литературы
1. Артеменко,А.И. Органическая химия: учеб. Для строит.вузов/ А.И.Артеменко. – 6-е изд., испр. – М.: Высш.шк., 2007.-539.с. 2. Писаренко,А.П. Курс органической химии: учебник для нехим.спец.вузов/ А.П.Писаренко, З.Я.Хавин. – 4-е изд., переб. И доп. – М.: Высш.шк., 1985.-527 с. 
12 Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
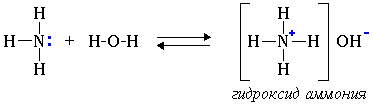



 или
или 