|
|
Приемы построения структурных формул изомеровРассмотрим на примере алкана С6Н14. 1. Сначала изображаем молекулу линейного изомера (ее углеродный скелет)
2.Затем цепь сокращаем на 1 атом углерода и этот атом присоединяем к какому-либо атому углерода цепи как ответвление от нее, исключая крайние положения:
Если присоединить углеродный атом к одному из крайних положений, то химическое строение цепи не изменится:
Кроме того, нужно следить, чтобы не было повторов. Так, структура
идентична структуре (2). 3.Когда все положения основной цепи исчерпаны, сокращаем цепь еще на 1 атом углерода:
Теперь в боковых ответвлениях разместятся 2 атома углерода. Здесь возможны следующие сочетания атомов:
Боковой заместитель может состоять из 2-х или более последовательно соединенных атомов углерода, но для гексана изомеров с такими боковыми ответвлениями не существует, и структура Боковой заместитель - С-С можно размещать только в цепи, содержащей не меньше 5-ти углеродных атомов и присоединять его можно только к 3-му и далее атому от конца цепи. 4.После построения углеродного скелета изомера необходимо дополнить все углеродные атомы в молекуле связями с водородом, учитывая, что углерод четырехвалентен. Итак, составу С6Н14 соответствует 5 изомеров: 1) 2) 5) Поворотная изомерия алканов Характерной особенностью s-связей является то, что электронная плотность в них распределена симметрично относительно оси, соединяющей ядра связываемых атомов (цилиндрическая или вращательная симметрия). Поэтому вращение атомов вокруг s-связи не будет приводить к ее разрыву. В результате внутримолекулярного вращения по s-связям С–С молекулы алканов, начиная с этана С2Н6, могут принимать разные геометрические формы. Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг s-связей С–С, называют конформациями или поворотными изомерами (конформерами). Поворотные изомеры молекулы представляют собой энергетически неравноценные ее состояния. Их взаимопревращение происходит быстро и постоянно в результате теплового движения. Поэтому поворотные изомеры не удается выделить в индивидуальном виде, но их существование доказано физическими методами. Некоторые конформации более устойчивы (энергетически выгодны) и молекула пребывает в таких состояниях более длительное время. Рассмотрим поворотные изомеры на примере этана Н3С–СН3:
При вращении одной группы СН3 относительно другой возникает множество неодинаковых форм молекулы, среди которых выделяют две характерные конформации (А и Б), отличающиеся поворотом на 60°:
Эти поворотные изомеры этана отличаются расстояниями между атомами водорода, соединенными с разными атомами углерода. В конформации А атомы водорода сближены (заслоняют друг друга), их отталкивание велико, энергия молекулы максимальна. Такая конформация называется "заслоненной", она энергетически невыгодна и молекула переходит в конформацию Б, где расстояния между атомами Н у разных атомов углерода наибольшее и, соответственно, отталкивание минимально. Эта конформация называется "заторможенной", т.к. она энергетически более выгодна и молекула находится в этой форме больше времени.
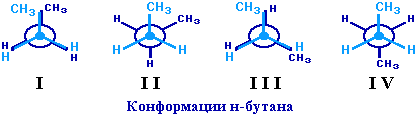
С удлинением углеродной цепи число различимых конформаций увеличивается. Так, вращение по центральной связи в н-бутане
приводит к четырем поворотным изомерам:
Наиболее устойчивым из них является конформер IV, в котором группы СН3 максимально удалены друг от друга. Зависимость потенциальной энергии н-бутана от угла вращения построить с учащимися на доске. Оптическая изомерия Если атом углерода в молекуле связан с четырьмя различными атомами или атомными группами, например:
то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами. Изомерия этого вида называется оптической, изомеры – оптическими изомерами или оптическими антиподами:
Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии. Таким образом, оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение. Оптические изомеры имеют одинаковые физические и химические свойства, но различаются отношением к поляризованному свету. Такие изомеры обладают оптической активностью (один из них вращает плоскость поляризованного света влево, а другой - на такой же угол вправо). Различия в химических свойствах наблюдаются только в реакциях с оптически активными реагентами. Оптическая изомерия проявляется в органических веществах различных классов и играет очень важную роль в химии природных соединений. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 (1)
(1) (2) или
(2) или  (3)
(3)


 (4) и
(4) и  (5)
(5) идентична структуре (3).
идентична структуре (3).
 3)
3)  4)
4)