
|
|
АКБ не должна храниться или длительно бездействовать в разряженном состоянии, т.е. аккумулятор должен быть всегда заряжен.Свинцовый аккумулятор был изобретен более 150 лет Гастоном Планте (в 1859-1860 годах), сотрудником лаборатории Александра Баккереля. Принцип действия аккумуляторов с тех пор принципиально не изменился и в усовершенствованной конструкции аккумуляторные батареи совершенно безотказно служит нам сегодня. В основе работы свинцового аккумулятора лежит химическая реакция (основная), которая представляется в следующем виде:
Т.е. под действием зарядного тока происходит поляризация свинцовых электродов и электролит (серная кислота – H2SO4 в смеси с водой – Н2О ) разлагается на кислород и водород. Продукты разложения вступают в реакцию со свинцом: на положительном электроде образуется двуокись свинца, а на отрицательном – губчатый свинец. Таким образом, возникает гальванический элемент с напряжением около 2 В. Как видно из основной формулы, процесс – обратимый, и при разряде в элементе происходит обратный процесс, когда химическая энергия переходит в электрическую. При этом из электролита снова выделяются кислород и водород. Последние вступают в реакцию с двуокисью свинца и губчатым свинцом, восстанавливая первую и окисляя второй. После достижения равновесного состояния, разряд прекращается. Однако после зарядки (обратного процесса) элемент опять готов к работе и так почти до бесконечности. Срок службы исчисляется тысячами циклов и годами эксплуатации (до 10 и более при надлежащем уходе). Так выглядят процессы в упрощенном виде, что вполне достаточно для их понимания. А в теории современных АКБ химики насчитывают более 60 реакций. Не будем вдаваться в подробности и повторим главное. И так: Процесс заряда. Протекание зарядного тока вызывает разложение электролита с выделением водорода, который переносится к отрицательному электроду, восстанавливает сульфат свинца до губчатого свинца с образованием серной кислоты. На положительном электроде образуется двуокись свинца. Серная кислота в этом процессе образуется, а вода расходуется, следовательно, плотность электролита повышается (серная кислота тяжелее воды). Процесс разряда. При включении аккумулятора под нагрузку, токи в элементах протекают от катода к аноду. Под воздействие тока потребления серная кислота частично разлагается и на положительном электроде выделяется водород. Происходит химический процесс образования сульфата свинца из двуокиси свинца на положительном электроде. Остаток частично разложившейся кислоты вступает в соединение с губчатым свинцом катода также до образования сульфата свинца. Очевидно, что в этом процессе серная кислота электролита расходуется, а в этом случае плотность электролита снижается (вода легче кислоты). На практике нужно учитывать, что процесс далеко не идеален, поскольку в циклах разряда-заряда происходят сопутствующие реакции, но для нас важен тот факт, что часть энергии расходуется на нагрев и гидролиз воды с выделением водорода и кислорода, особенно в случае перезаряда АКБ. В противном случае к.п.д. аккумулятора был бы равен 1 (100%), чего природа не допускает и в лучших образцах он достигает чуть более 80% . Учтем этот факт и рассмотрим конструкцию аккумуляторной батареи. Как мы выяснили, один свинцовый кислотный аккумуляторный элемент способен выдавать напряжение приблизительно 2 вольта. В зависимости от требуемого напряжения батареи, элементы соединяются последовательно. Так для обеспечения U= 6 В потребуется соединение трех элементов, для U= 12 В – шести, 24 В – 12- ти или двух 12Вольтовых и т.д. Наибольшее распространение для автомобильной технике получили 12В АКБ и таковых выпускается подавляющее большинство. Устройство такой аккумуляторной батареи показано на рис. 1.
Рис. 1 АКБ состоит из корпуса, в котором сформованы изолированные друг от друга банки всего 6 штук для установки аккумуляторных элементов. Аккумуляторные элементы погружены в отдельные банки и соединены друг с другом межэлементными соединениями. Корпус накрыт крышкой, стык герметизирован. Для каждой банки в крышке отформованы заливные горловины, которые закрываются резьбовыми пробками с отверстиями для вентиляции. Через крышку выведены клеммы аккумулятора. Клеммы АКБ замаркированы и если они конусные, то плюсовая клемма имеет больший диаметр. Переполюсовка аккумуляторных батарей возможна, но крайне не желательна. Положение и конфигурация выводов, в принципе, м.б. любой, в зависимости от требований заказчика. Каждый элемент состоит из набора пластин. Пластины изготовлены из свинца в виде решетки и обмазаны активной массой. На отрицательных пластинах активной массой является губчатый свинец, а на положительных нанесена активная масса из оксида свинца. Поэтому пластины отличаются по цвету – губчатый свинец (отрицательная пластина) имеет серый цвет, а положительная – коричневый. Каждая из пластин имеет специальный прилив – борн, который обеспечивает межэлементное соединение как внутри каждой банки элемента, так и соединение элементов в батарею. Во избежание касаний последовательно установленных пластин разной полярности (короткого замыкания) в результате их деформации, возможной в процессе эксплуатации, между ними устанавливается изолирующий перфорированный сепаратор, не препятствующий протеканию электролита. Для производства корпусов аккумуляторных батарей используются кислотостойкие электроизоляционные материалы. На протяжении длительного времени основным материалом являлся эбонит. В настоящее время от него отказываются, и все шире используют более дешевые, надежные и технологичные пластполимерные массы. Что касается самих электродов, то их состав достаточно разнообразен и строго регламентирован в плане использования присадок, способствующих улучшению свойств электродов (сурьма, кальций, селен и др.) и строгого контроля отсутствия вредных примесей (хлор, марганец и пр.). Чем чище производство и используемые материалы, тем качественнее будет АКБ и тем дольше будет срок ее службы. Далее кратко об основных характеристиках аккумулятора. Рассматривая характеристики, в первую очередь, необходимо упомянуть о рабочей емкости. Рабочая емкость аккумулятора это то количество электричества, которое способна отдать АКБ в определенном режиме разряда до предельного для данного режима разряда напряжения. Эта емкость еще называют номинальной и измеряют в ампер-часах. Считается, что при 20 часовом разряде током, численно равным 0, 05 номинальной емкости напряжение на клеммах не должно быть ниже 10,5 В при температуре электролита 25оС. Полная емкость аккумулятора значительно больше номинальной, однако отбирать полную емкость от аккумулятора нельзя, так как это приведет к его невосполнимому истощению. Работа аккумулятора после отбора номинальной рабочей емкости - запретная экстремальная работа аккумулятора в аварийном режиме. Заметное влияние на емкость аккумулятора оказывает температура электролита. При увеличении температуры свыше 25оС на каждый градус приходится приблизительно 1% увеличения емкости, а при понижении температуры до 5оС, аккумулятор может потерять до 30% номинальной емкости. Этому есть свое физическое объяснение: с повышением температуры снижается вязкость электролита, а, следовательно, усиливается диффузия его в поры активной массы пластин (химические реакции протекают в большем объеме и с большей скоростью). При этом происходит снижение внутреннего сопротивление аккумулятора, как источника напряжения в замкнутой цепи. В этой связи рассмотрим еще один, особенно актуальный для стартерных батарей – ток холодной прокрутки. По ГОСТ 959-2002 это ток разряда, который способна отдать батарея при температуре электролита минус 18оС (-18оС) в течение 10 секунд с напряжением не менее 7.5 В. Принимая во внимание рассмотренные физическо-химические процессы и конструктивные особенности, из всего вышесказанного вытекают следующие требования к безопасности и правила эксплуатации, обслуживания и ремонта аккумуляторных батарей и элементов. Во-первых! Никогда нельзя забывать о том, что протекание химических реакций в аккумуляторных элементах сопровождаются выделением водорода, особенно опасным это становится при перезаряде аккумулятора от источника тока, когда начинается гидролиз воды. Водород в соединении с кислородом создают гремучую смесь, способную взорваться от любого источника, будь то искра, нагретые до высоких температур поверхности или источники открытого пламени. Поэтому никогда не производите какие либо манипуляции с аккумуляторами на зарядке или при их работе. В случае необходимости, прежде чем отключать аккумулятор, не торопитесь и дайте ему некоторое время постоять для того чтобы концентрация водорода понизилась ниже взрывоопасного предела (желательно около 1 часа). Обслуживание аккумуляторов нужно производить в хорошо вентилируемых помещениях, на крайний случай, установите вентилятор для создания потока воздуха. Поверьте, пренебрежение мерами по удалению водорода способно вызвать взрыв аккумулятора, а это совершенно незабываемое зрелище с разбрызгиванием достаточно концентрированного раствора серной кислоты! Во-вторых, при монтаже и демонтаже батареи или элементов никогда не забывайте, что имеете дело с источником напряжения. А это значит, что при определенных условиях возможно поражение электрическим током. В-третьих, в случае протекания в батарее разрядного или зарядного тока отключение потребителей или зарядного устройства способно вызвать искрообразование (и далее см. п. Во-первых). Если система однопроводная, что встречается достаточно часто, то первым должен сниматься контакт «массы» (обычно минус), поскольку касание ключом или съемником окружающего металла в этом случае не вызовет короткого замыкания батареи. Напротив, при монтаже, первым подсоединяется провод к «не массовой» клемме (обычно плюсовой), в противном случае касание используемого инструмента «массы» вызовет КЗ (при уже подсоединенном проводе к «массовой» клемме). В четвертых, не менее важным при эксплуатации и обслуживании аккумуляторов является понимание того, что вы имеете дело с достаточно вредными для здоровья веществами: ядовитым является как основной материал пластин – свинец, так и присадки для улучшения свойств – мышьяк, сурьма. Не меньший вред может нанести и электролит – водный раствор концентрированной серной кислоты. Попадание паров или частиц свинцового сплава в дыхательные пути крайне опасно, поэтому при очистке клемм аккумулятора необходимо одеть респиратор, а после работ рекомендуется прополоскать рот водой. При работе с серной кислотой нужно избегать использование в одежде синтетических материалов, отдавая предпочтение грубым шерстяным вещам, а также пользоваться прорезиненным передником, резиновыми перчатками, сапогами и защитой для лица (хотя бы для глаз). В случае попадания кислоты на открытые участки кожи промокнуть чистой технической салфеткой, тщательно промыть водой и немедленно обработать (нейтрализовать) 5%-ым раствором двууглекислой соды. В случае попадания кислоты на слизистую оболочку или в глаза, их необходимо промыть 2 – 3% -ым раствором пищевой соды. Поэтому наличием этих растворов следует озаботиться заранее и иметь необходимые ингредиенты «под рукой». И, наконец, последнее: в том случае, если вам потребуется приготовление электролита, не в коем случае не вливайте воду для разбавления в кислоту. Дело в том. Что при смешивании выделяется большое количество теплоты и вода, обладающая более высокой теплопроводностью и более низкой температурой кипения, чем кислота, вскипит и вызовет разбрызгивание кислоты. Поэтому необходимо посудину для приготовления электролита сначала заполнить водой, в которую при непременном перемешивании добавлять кислоту. В этом случае выделяемая теплота будет поглощена водой и смешивание произойдет без разбрызгивания. Водой допускается разбавлять электролит только с плотностью не более 1,28 г/см3. Во избежание эксцессов эти правила нужно запомнить! А теперь перейдем к правилам эксплуатации и обслуживания АКБ. Равно как и меры безопасности, изложенные выше, правила эксплуатации предопределены особенностями физико-химических процессов, происходящих в аккумуляторе. Для начала вспомним, что в процессе разряда аккумулятора, продуктом реакции является сульфат свинца, который оседает на пластинах. Сульфат свинца это соль, которая имеет вид серой кашицы и появление ее в процессе разряда свинцового аккумулятора совершенно естественный процесс. В процессе зарядки аккумулятора сульфат восстанавливается с образованием губчатого свинца и серной кислоты. Все это было бы хорошо, если бы сульфат свинца, как любая другая соль, не обладал пагубной способностью с течением времени кристаллизоваться. И вот тогда начинаются проблемы. Кристаллы начинают препятствовать попаданию реагентов в зоны реакции в объеме пластин, т.е. часть поверхности пластин выключаются из работы, и, как следствие, аккумулятор начинает катастрофически терять емкость. Этот крайне негативный процесс так и называют: «сульфатация». Отсюда напрашивается вывод, который сформулируем первым основным правилом. АКБ не должна храниться или длительно бездействовать в разряженном состоянии, т.е. аккумулятор должен быть всегда заряжен. Определить степень заряженности (или разряженности) аккумуляторной батареи можно на основе анализа плотности электролита в банках составляющих ее элементов. Плотность электролита, которым заправлены элементы, указывается в паспорте на аккумулятор и обычно составляет 1,24 – 1.28 г/см3. Номинальная плотность электролита в заряженной батарее задается изготовителем из условий эксплуатации – чем холоднее, тем выше плотность. Для измерения плотности используется специальный прибор – ареометр. Если номинальная плотность не известна, то не будет вреда от зарядки батареи и, если плотность электролита в течение ≈ 1 – 1,5 часов зарядки от источника тока остается неизменной, а в элементах происходит равномерное “кипение” электролита, то батарея заряжена полностью и плотность электролита – номинальная. При этом напряжение на клеммах элементов должно быть равномерным и составлять 2,1 – 2,2 В/эл. Ток зарядки батареи (при отсутствии иных указаний) можно назначать из тех соображений, что номинальная емкость полностью разряженного аккумулятора восстанавливается за 8 – 10 часов. При проведении зарядки АКБ необходимо контролировать температуру электролита. Повышенный ток зарядки может привести к перегреву аккумулятора, короблению пластин и их осыпанию. Таким образом, аккумулятору будет нанесено серьезное повреждение, и такой поврежденный аккумуляторный элемент восстановлению не подлежит. Температура электролита не должна превышать 40оС. В случае достижения этой температуры процесс зарядки следует немедленно прекратить. Одновременно нельзя забывать, что плотность электролита, как и плотность любого другого вещества, зависит от температуры и для определения номинальной плотности (при 20оС) нагретого электролита потребуется не сложный пересчет по простой формуле:
где:
В целом необходимо отметить, что температура эксплуатации аккумуляторных батарей весьма критичный параметр. При хранении аккумуляторной батареи (равно как и в случае невостребованности разряда при ее работе) в батарее протекает слабый ток – ток саморазряда. Этот процесс неизбежен и с ним приходится мириться. (Именно в этой связи требуется контроль плотности и периодическая подзарядка.) Однако саморазряд аккумулятора при снижении температуры электролита заметно уменьшается. Поэтому желательно, чтобы температура окружающей аккумулятор среды была по возможности более низкой. Правда, нужно учитывать, что температура замерзания электролита плотностью 1,21 г/см3 составляет –27оС, для электролита 1,24 г/см3 – минус 48оС, а замерзание электролита в АКБ не допустимо. Напротив, повышенные температуры выше 20оС приводит к снижению срока службы аккумулятора. В отдельных случаях превышение регламентированной изготовителем предельной температуры эксплуатации на 10оС способно сократить срок службы вдвое, а на 20оС – в четыре раза. Продолжая разговор о саморазряде аккумуляторов, нужно отдельно упомянуть, что АКБ должна обязательно содержаться в полной чистоте. Учитывая то, что электролит это токопроводящая среда, поверхность крышки в случае попадания на нее электролита при «кипении» на зарядке, превратится в проводник и ток саморазряда аккумулятора увеличится. Поэтому периодически аккумулятор требует очистки и нейтрализации поверхности корпуса и крышки путем протирки поверхностей 10% раствором соды. А с клемм необходимо удалять следы коррозии и консервировать контакты нанесением специальной консистентной смазки. В случае образования кристаллической сульфидной пленки на поверхности пластин (сульфатации) аккумулятор теряет емкость, и плотность электролита понижается. АКБ можно пробовать «реанимировать» путем проведения десульфатационных тренировочных циклов разряда – заряда слабыми токами. Плотность электролита в банках может изменяться, в основном за счет испарения и гидролиза воды при работе батареи. Поэтому необходимо производить контроль уровня электролита и плотности. В случае необходимости восстановления уровня в банки добавляют дисцилированную воду. Как уже упоминалось ранее, аккумуляторные элементы требуют использования только чистых материалов и внесение любых примесей с водой могут оказаться фатальными. Также возможна ситуация, когда требуется корректировка плотности электролита в сторону повышения, тогда нужно воспользоваться корректирующим электролитом с плотностью 1,3 г/см3. Нужно четко отдавать себе отчет в действиях при корректировке плотности и не поднимать плотность электролита до выяснения причин ее понижения. Принципиально, плотность электролита во всех банка аккумуляторной батареи должна быть одинаковой. В противном случае, изменение плотности в одной из банок свидетельствует о неисправности этого аккумуляторного элемента. Наиболее распространенной причиной этому является осыпание пластин. Осыпавшаяся обмазка накапливается на дне банки и при достижении уровня расположения пластин происходит замыкание элемента. В результате элемент разряжается, плотность электролита падает, а вся батарея не способна выдать требуемое напряжение при одновременной потере емкости. Если аккумулятор обслуживаемый, то банку можно промыть или заменить, но это уже капитальный ремонт, выполнение которого не всегда целесообразно и экономически оправдано. Следующий пункт проверки технического состояния – проверка изоляции. В зависимости от номинального напряжения сопротивление изоляции должно быть не менее значений, указанных в таблице 1. Таблица 1. Технические требования к сопротивлению изоляции
Сопротивление изоляции аккумуляторных батарей положено измерять не реже 1 раза в 3 месяца. Подытожим сказанное. При проведении периодического осмотра АКБ необходимо проверять: 1. Напряжение батареи, плотность и температуру электролита. 2. Напряжение и ток подзаряда. 3. Целостность корпусов и крышек, отсутствие течи электролита, чистоту АКБ, отсутствие коррозии на клеммах, зажимах, перемычках и др. При необходимости очистить и смазать техническим вазелином. 4. Уровень электролита и его цвет. 5. Отсутствие сильного газовыделения («кипения») в банках аккумулятора. 6. Уровень и цвет шлама если корпус прозрачный. Профилактический контроль аккумуляторных батарей на предмет определения их работоспособности и состояния предусматривает анализ проб электролита. Пробы отбирают после разряда аккумулятора, поскольку концентрация вредных примесей в этом случае максимальна. Визуально электролит должен быть прозрачным и бесцветным. К числу видимых признаков неудовлетворительного качества электролита относится его цвет. Цвет от светлого до темно-коричневого свидетельствует о присутствии органических соединений, которые во время эксплуатации АКБ быстро переходят в уксуснокислые соединения; фиолетовый (м.б. малиновый) цвет указывает на присутствие соединений марганца. Применение электролита с содержанием примесей выше допустимых норм причиняет: - значительный саморазряд при наличии меди, железа, мышьяка сурьмы, висмута; - увеличение внутреннего сопротивления при наличии марганца; - разрушение положительных электродов вследствие наличия остовой и/или азотной кислот или их производных; - разрушение положительных и отрицательных электродов под воздействием соляной кислоты или/и хлорсодержащих соединений. В случае обнаружения вредных примесей, загрязненный электролит сливают из разряженного аккумулятора вместе со шламом. Если аккумулятор загрязнен железом, то аккумулятор промывают дистиллированной водой, затем заливают электролит пониженной плотности (порядка 1,05 г/см3), заряжают АКБ до постоянной плотности электролита, потом раствор сливают, аккумулятор заправляют свежим электролитом нормальной плотности и если повторный отбор пробы после разряда не дает положительный результат, процедуру повторяют. Если электролит загрязнен марганцем, достаточно на разряженном аккумуляторе поменять электролит на свежий и снова зарядить АКБ. Попавшую в аккумулятор медь удалить с электролитом не удастся, ее можно удалить только с отрицательными электродами, на которые она переносится при зарядке. Надеюсь, теперь понятно, как следует относиться к чистоте материалов и рабочего места! Основные неполадки и методы устранения их в ходе проведения текущего ремонта сведены в табл. 2 Таблица 2
Что касается вопросов капитального ремонта АКБ, то к работам в объеме капитального ремонта относятся: замена электродов или элементов в составе батареи; восстановление контактных выводов; ремонт корпусов и др. Однако необходимо отметить, что, ввиду специфики, выполнение таких работ должно производиться на специализированных предприятиях. Кроме того, современные аккумуляторные батареи сконструированы таким образом, что требуют минимум затрат на обслуживание и ремонт таких батарей не представляется целесообразным, а после выработки ресурса они просто подлежат замене. Более того, в последнее время все более широкое распространение получают так называемые необслуживаемые аккумуляторы, которые, благодаря использованию специальных материалов-присадок к материалу электродов, менее склонны к «выкипанию» и даже не требуют пополнения банок дистиллированной водой в течение всего периода эксплуатации. Крышки корпуса таких батарей даже не имеют пробок для контроля и корректировки плотности электролита, а только организован газоотвод от банок, скорее для компенсации перепадов давления при нагреве. В заключении необходимо упомянуть, что кислотные свинцовые аккумуляторы хоть и превалируют на рынке, но не являются единственными. Достаточно широко также используются щелочные аккумуляторы. Щелочные аккумуляторы обладают рядом преимуществ, по сравнению с кислотными, к наиболее весомыми относятся: - устойчивость к механическим и вибрационным нагрузкам; - при прочих равных условиях, разрядные токи могут иметь большие значения; - легче и меньше при равных емкостях; - имеют более высокий ресурс работы; - менее критичны к недозарядам и перезарядам; - более просты в эксплуатации. Но достоинств в технике без недостатков не бывает. Так, из-за использования дорогостоящих материалов (в частности - серебра) щелочной аккумулятор может оказаться в четыре и более раз дороже, чем кислотный свинцовый аналог. Кроме того напряжение на элементе щелочного аккумулятора составляет всего 1,25 В, а это, в ряде случаев, усложняет конструкцию. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|


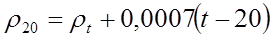
 - плотность электролита при температуре 20оС, г/см3;
- плотность электролита при температуре 20оС, г/см3; - измеренная плотность электролита при температуре
- измеренная плотность электролита при температуре  , г/см3;
, г/см3; - температура электролита, при которой проводилось измерение плотности, оС.
- температура электролита, при которой проводилось измерение плотности, оС.