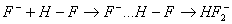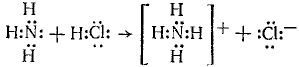|
|
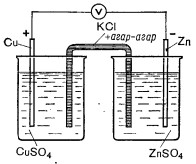
Донорно-акцеторная связь.12 Принцип работы гальванического элемента. Принцип действия гальванического элемента. В два стакана наливают до половины 1 М раствора сульфата меди и сульфата цинка. В первый стакан погружают медную пластинку, во второй ‒ цинковую (рис.). Растворы в стаканах соединяют U-образной трубкой, заполненной электролитом - раствором хлорида калия, основой которого является 5-процентный раствор агар-агара.
Рис. Схема медно-цинкового гальванического элемента U-образная трубка (сифон) является соединительным мостиком для того, чтобы ионы могли свободно перемещаться из раствора одного стакана в другой. Свободные концы проводников от электродов присоединяют к гальванометра, указывающий на появление электрического тока в гальваническом ночном элементе. Э. д. с. (Электродвижущую силу) элемента можно определить с помощью вольтметра или рассчитать, пользуясь таблицей нормальных электродных потенциалов. Zn | Zn2+ — 76 В; Сu | Сu2+ = +34 В; ЭДС = +0,34 В ‒( ‒ 0,76 В) =1,1 В. Полученная Э. д. с. гальванического элемента может значительно отличаться от действительной. Точность измерения зависит от сопротивления вольтметра, диаметра U-образной трубки. Чем больше диаметр трубки, тем точнее результат. Отметим, что для точного измерения Э. д. с. лучше использовать компенсационные схемы, в частности приборы, основанные на этой схеме, ‒ потенциометры. Приготовление раствора электролита для U-образной трубки: 5 г агар-агара растворяют в 95 г воды при нагревании. В растворе агар-агара растворяют 25 г хлорида калия. Реактивы и оборудование: сульфат меди СuSO4, сульфат цинка ZnSO4, хлорид калия КС1, агар-агар, 2 стакана на 250 мл, цинковая и медная пластинки (12 см×2 см) с припаянными проводниками, вольтметр, U-образная стеклянная трубка диаметром 5 -7 мм.
Межмолекулярные взаимодействия. Межмолекулярные взаимодействия, взаимодействия молекул между собой, не приводящее к разрыву или образованию новых химических связей. Межмолекулярные взаимодействия определяют отличие реальных газов от идеальных, существование жидкостей и молекулярных кристаллов. От межмолекулярных взаимодействий зависят многие структурные, спектральные, термодинамические, теплофизические и другие свойства веществ. Появление понятия межмолекулярные взаимодействия связано с именем Й. Д. Ван-дер-Ваальса, который для объяснения свойств реальных газов и жидкостей предложил в 1873 уравнение состояния, учитывающее межмолекулярные взаимодействия. Поэтому силы межмолекулярного взаимодействия часто называют ван-дер-ваальсовыми. Виды межмолекулярных взаимодействий.Основу межмолекулярных взаимодействий составляют кулоновские силы взаимодействия между электронами и ядрами одной молекулы и ядрами и электронами другой. В экспериментально определяемых свойствах вещества проявляется усредненное взаимодействие, которое зависит от расстояния R между молекулами, их взаимной ориентации, строения и физических характеристик (дипольного момента, поляризуемости и др.). При больших R, значительно превосходящих линейные размеры l самих молекул, вследствие чего электронные оболочки молекул не перекрываются, силы межмолекулярного взаимодействия можно достаточно обоснованно подразделить на три вида - электростатические, поляризационные (индукционные) и дисперсионные. Электростатические силы иногда называют ориентационными, однако это неточно, поскольку взаимная ориентация молекул может обусловливаться также и поляризационными силами, если молекулы анизотропны. При малых расстояниях между молекулами (R ~ l) различать отдельные виды межмолекулярных взаимодействий можно лишь приближенно, при этом, помимо названных трех видов, выделяют еще два, связанные с перекрыванием электронных оболочек, - обменное взаимодействие и взаимодействия, обязанные переносу электронного заряда. Несмотря на некоторую условность, такое деление в каждом конкретном случае позволяет объяснять природу межмолекулярного взаимодействия и рассчитать его энергию. Водородная связь. Водородная связь - это своеобразная химическая связь. Она может быть межмолекулярной и внутримолекулярной. Межмолекулярная водородная связь возникает между молекулами, в состав которых входят водород и сильно электроотрицательный злемент - фтор, кислород, азот, реже хлор, сера. Поскольку в такой молекуле общая электронная пара сильно смещена от водорода к атому электроотрицательного элемента, а положительный заряд водорода сконцентрирован в малом объеме, то протон взаимодействует с неподеленной электронной парой другого атома или иона, обобществляя ее. В результате образуется вторая, более слабая связь, получившая название водородной. Обычно водородную связь обозначают точками и этим указывают, что она намного слабее ковалентной связи (примерно в 15-20 раз). Тем не менее она ответственна за ассоциацию молекул. Например, образование димеров (в жидком состоянии они наиболее устойчивы) воды и уксусной кислоты можно представить схемами:
H - O....H - O | | H H (H2O)2
O....H - O // \ CH3 - C C - CH3 \ // O - H....O
(CH3COOH) 2
Как видно из этих примеров, посредством водородной связи объединены две молекулы воды, а в случае уксусной кислоты - две молекулы кислоты с образованием циклической структуры. Водородная связь оказывает влияние на свойства многих веществ. Так, благодаря водородной связи фтороводород в обычных условиях существует в жидком состоянии (ниже 19,5оС) и содержит молекулы состава от Н2F2 до Н6F6. Благодаря водородной связи образуется гидродифторид-ион который входит в состав солей - гидрофторидов (КНF2 - гидродифторид калия, NH4HF2 - гидродифторид аммония). Наличием водородных связей объясняется более высокая температура кипения воды (100оС) по сравнению с водородными соединениями элементов подгруппы кислорода (Н2S, Н2Sе, Н2Те). В случае воды надо затратить дополнительную энергию на разрушение водородных связей. Особенно распространены водородные связи в молекулах белков, нуклеиновых кислот и других биологически важных соединений, а потому эти связи играют важную роль в химии процессов жизнедеятельности. Металлическая связь. Металлы объединяют свойства, имеющие общий характер и отличающиеся от свойств других веществ. Такими свойствами являются сравнительно высокие температуры плавления, способность к отражению света, высокая тепло- и электропроводность. Эти особенности обязаны существованию в металлах особого вида связи — металлической связи. Металлическая связь— связь между положительными ионами в кристаллах металлов, осуществляемая за счет притяжения электронов, свободно перемещающихся по кристаллу. В соответствии с положением в периодической системе атомы металлов имеют небольшое число валентных электронов. Эти электроны достаточно слабо связаны со своими ядрами и могут легко отрываться от них. В результате в кристаллической решетке металла появляются положительно заряженные ионы и свободные электроны. Поэтому в кристаллической решетке металлов существует большая свобода перемещения электронов: одни из атомов будут терять свои электроны, а образующиеся ионы могут принимать эти электроны из «электронного газа». Как следствие, металл представляет собой ряд положительных ионов, локализованных в определенных положениях кристаллической решетки, и большое количество электронов, сравнительно свободно перемещающихся в поле положительных центров. В этом состоит важное отличие металлических связей от ковалентных, которые имеют строгую направленность в пространстве. Металлическая связь отличается от ковалентной также и по прочности: ее энергия в 3-4 раза меньше энергии ковалентной связи. Энергия связи — энергия, необходимая для разрыва химической связи во всех молекулах, составляющих один моль вещества. Энергии ковалентных и ионных связей обычно велики и составляют величины порядка 100-800 кДж/моль. Донорно-акцеторная связь. Донорно-акцепторная связь (координационная связь, семиполярная связь) — химическая связь между двумя атомами или группой атомов, осуществляемая за счет неподеленной пары электронов одного атома (донора) и свободного уровня другого атома (акцептора). Донорно-акцепторная связь образуется часто при комплексообразовании за счет свободной пары электронов, принадлежавшей (до образования связи) только одному атому (донору). Донорно-акцепторная связь отличается от обычной ковалентной только происхождением связевых электронов. Реакция аммиака с кислотой состоит в присоединении протона, отдаваемого кислотой, к неподеленным электронам азота:
В ионе NH4+ все четыре связи азота с водородом равноценны, хотя отличаются происхождением. Донорами могут быть атомы азота, кислорода, фосфора, серы и др. Роль акцепторов могут выполнять протон, а также атомы с незаполненным октетом, напр. атомы элементов III группы таблицы Д. И. Менделеева, а также атомы-комплексообразователи, имеющие незаполненные энергетические ячейки в валентном электронном слое. Донорно-акцепторная связь называется иначе семиполярной (полуполярной), так как на атоме-доноре возникает эффективный положительный заряд, а на атоме-акцепторе — эффективный отрицательный заряд. Изображают эту связь стрелкой, направленной от донора к акцептору. Ионная связь. Химическая связь, основанная на электростатическом притяжении ионов, называется ионной связью. Такая связь возникает при большой разнице в электроотрицательностях связываемых атомов (Δχ > 2 ), когда менее электроотрицательный атом почти полностью отдает свои валентные электроны и превращается в катион, а другой, более электроотрицательный атом, эти электроны присоединяет и становится анионом. Например, в хлориде натрия NaCl разность электроотрицательностей атомов равна: Δχ = 3,0(Cl) - 0,9(Na) = 2,1 Атом Na (1 электрон на внешнем уровне) и атом Cl (7 внешних электронов) превращаются в ионы Na+ и Cl– с завершенными внешними электронными оболочками (по 8 электронов), между которыми возникает электростатическое притяжение, т.е. ионная связь. Иoннaя связь не имеет пространственной направленности, так как каждый ион связан с некоторым числом противоионов, сила действия которых зависит от расстояния (закон Кулона). Поэтому ионно-связанные соединения не имеют молекулярного строения и представляют собой твердые вещества, образующие ионные кристаллические решетки, с высокими температурами плавления и кипения, они высокополярны, часто солеобразны, в водных растворах электропроводны. Соединений с чисто ионными связями практически не существует. В органических соединениях ионные связи встречаются довольно редко, т.к. атом углерода не склонен ни терять, ни приобретать электроны с образованием ионов. Тем не менее, ионная связь присутствует в соединениях, где заряд локализован на гетероатомах (например, в органических солях RCOO–Na+, RO–K+, R4N+Cl– и основаниях R4N+OH–). 
12 Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 :
: