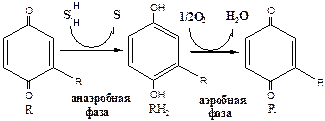|
|
Современные представления о биологическом окисленииКафедра биохимии Утверждаю Зав. каф. проф., д.м.н. Мещанинов В.Н. _____‘’_____________2005 г ЛЕКЦИЯ № 4 Тема: биологическое окисление: этапы, цикл Кребса, Пути использования кислорода в тканях. Факультеты: лечебно-профилактический, медико-профилактический, педиатрический. 2 курс.
История развития учения о биологическом окислении Изучение окисления в организме было начато в 18 в. А. Лавуазье; в дальнейшем значительный вклад в исследование БО (его локализация в живых клетках, связь с др. процессами обмена веществ, механизмы ферментативных окислительно-восстановительных реакций, аккумуляция и превращение энергии и др.) внесли О. Варбург, Г. Виланд (Германия), Д. Кейлин, Х. Кребс, П. Митчелл (Великобритания), Д. Грин, А. Ленинджер, Б. Чанс, Э. Рэкер (США), а в СССР - А. Н.Бах, В. И. Палладин, В. А. Энгельгардт, С. Е. Северин, В. А. Белицер, В. П. Скулачев и др. В 1777г французский химик Антуан ЛоранЛавуазье (1743-1794), впервые правильно истолковал явление горения как процесс соединения веществ с О2. Так как горение и дыхание сопровождаются потреблением О2 и выделение СО2, он предположил что, в их основе лежит один процесс. Однако у дыхания были существенные отличия от горения: оно шло при низкой температуре, без пламени и в присутствии воды. В конце XIX века русские исследователи А.Н. Бах и В.И. Палладин, работая независимо друг от друга, предложили 2 основные теории для объяснения процессов, протекающих в ходе биологического окисления. В 1897г Алексей Николаевич Бах (1857-1946) сформулировал «перекисную теорию медленного окисления», согласно которой молекула О2 сначала активируется. Активация О2 происходит в результате разрыва одной его связи (-О-О-) и присоединения к органическим веществам – оксидазам. Активированный О2 при взаимодействии с окисляемым веществом образует перекись.
Теория «перекисного окисления» Баха нашла свое подтверждение, однако главный механизм БО оказался иным. Важнейшая заслуга в развитии учения о БО принадлежит русскому ученому ботанику и биохимику В.И.Палладину (1859-1922), который создал теорию «активации водорода». Он предположил, что окисление субстратов может происходить в 2 стадии. 1). Анаэробная фаза. В этой фазе особые вещества хромогены (R) отщепляют Н от субстратов и восстанавливаются (RH2). 2). Аэробная фаза. Восстановленные хромогены RH2 передают Н на О2.
В последствии теория В.И. Паладина блестяще подтвердилась для процессов митоходриального окисления, а ферменты, принимающие непосредственное участие в отнятии водорода от субстратов, в настоящее время называются дегидрогеназами. Современные представления о биологическом окислении Согласно современной теории БО, окисление происходит как в аэробных, так и в анаэробных условиях. В аэробных организмах существует несколько путей использования О2. Реакции БО необходимы для получения энергии, синтеза новых веществ и разрушения чужеродных веществ. БО является сложным, многостадийным процессом, в котором ведущую роль играют ферменты оксидоредуктазы. Окислительно-восстановительные реакции(ОВР) – реакции, в которых меняется степень окисления субстрата за счет присоединения/отщепления: 1) 1 е-; 2) 2е- и 2Н+; 3) атомов кислорода. Биологическое окисление (БО) совокупность окислительно-восстановительных реакций, которые протекают во всех живых клетках. Основная функция БО - обеспечение организма энергией в доступной для использования форме (АТФ). Субстрат БО – вещество, способное отдавать электрон. Тканевое дыхание – окисление органических веществ в клетках, сопровождающееся потреблением О2 и выделением воды. Субстрат тканевого дыхания – это вещество, которое отдает электрон непосредственно в цепь окислительного фосфорилирования. Дыхательная цепь – цепь переноса электронов. В переносе электронов от субстратов БО к О2 принимают участие: 1) НАД и НАДФ зависимые ДГ; 2) ФАД и ФМН зависимые ДГ; 3) цитохромы; 4) коэнзим Q; 5) белки, содержащие негеминовое железо. Свободная энергия. Каждое органическое вещество обладает определенным запасом внутренней энергии (Е). Часть этой внутренней энергии может быть использована для совершения полезной работы, такую энергию называют свободной (G). Направление химической реакции определяется значением ∆G. У катаболических реакций ∆G отрицательно, эти реакции протекают самопроизвольно (экзергонические реакции). У анболических реакций ∆G положительно, они протекают только при поступлении свободной энергии извне (эндергонические реакции). Редокс-потенциалы. В каждой окислительно-восстановительной системе участвует окисленная и восстановленная формы одного соединения, которые образуют сопряженную окислительно-восстановительную или редокс-пару. Разные редокс-пары обладают различным сродством к электрону. Мерой сродства редокс-пары к электрону служит окислительно-восстановительный потенциал, или редокс-потенциал (Ео'), величина которого прямо пропорциональна изменению свободной энергии ∆G. Величину Ео' выражают в вольтах; чем она отрицательнее, тем меньше сродство вещества к электронам и наоборот. Самое низкое сродство к электрону -0,42В у водорода. Самое высокое сродство к электрону +0,82В у О2. Компоненты дыхательной цепи имеют редокс-потенциалы, занимающие промежуточное положение между -0,42В и +0,82В. В дыхательной цепи, вещества переносящие электрон, располагаются в порядке увеличения их редокс-потенциала. Электрон перемещается по дыхательной цепи от веществ с низким сродством к электрону к веществам с более высоким сродством к электрону, при этом происходит высвобождение свободной энергии, часть которой фиксируется в виде макроэргических соединений. Электроны в дыхательную цепь поставляют субстраты тканевого дыхания. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|