
|
|
Порядок выполнения работыЛабораторная работа №4 Цель работы: изучение спектрального метода исследования веществ с использованием спектроскопа; определение длин волн спектральных линий атома водорода; расчет постоянной Ридберга. Приборы и оборудование: монохроматор УМ-2, работающий в режиме спектроскопа; конденсор; неоновая лампа; ртутная лампа ДРШ; водородная трубка; высокочастотный генератор. Краткая теория
Спектральный анализ – это физический метод определения качественного и количественного состава вещества на основе изучения его спектров. Совокупность частот (или длин волн), содержащихся в излучении вещества, называется спектром испускания данного вещества. Спектр излучения отдельных атомов состоит из отдельных спектральных линий - линейчатый спектр. Молекулярные спектры в отличие от атомных представляют собой набор полос – полосатый спектр. В задачу данной работы входит изучение линейчатого спектра испускания водорода в газообразном состоянии с помощью спектроскопа. Как же возникает линейчатый спектр излучения отдельных атомов водорода? Прежде всего происходит диссоциация молекул на атомы в газовом разряде в результате столкновений свободных электронов с молекулами. Далее соответствующие столкновения свободных электронов с атомами обуславливают переход электрона в атоме на более высокие энергетические уровни. Такое состояние атома или молекулы, возникающее при рекомбинации атомов, не является устойчивым, через время ~10-8 с электрон вернется на свой энергетический уровень, и атом или молекула испустят квант света - фотон. Основным будет линейчатый спектр испускания атомов водорода, на который может частично накладываться менее интенсивный полосатый спектр молекул водорода. Согласно второму постулату Бора, энергия фотона, который испускается при переходе электрона в атоме из состояния с номеромm в состояние с номеромn, равна
или где Из квантовой механики следует, что энергии электронов в атомах могут принимать только определенные дискретные значения. Состояния, отвечающие этим значениям энергии, называются энергетическими уровнями. При переходе электронов на более низкие уровни излучаются спектральные линии. Совокупность линий, отвечающих переходам с различных более высоких уровней на один и тот же нижний уровень, образует спектральную серию. Наиболее простой является система энергетических уровней атома водорода. Значение энергий электрона в атоме водорода можно вычислить по формуле:
где n – главное квантовое число, Из (1) и (2) следует, что длины волн спектральных линий атома водорода могут быть рассчитаны по формуле:
где – константа, называемая постоянной Ридберга. Формула (3) называется обобщенной формулой Бальмера. Из формулы (3) следует, что линии в спектре атома водорода можно расположить по сериям. Для всех линий одной и той же серии значение n остается постоянным, а m может принимать любые целые значения, начиная с (n + 1). В данной работе изучается серия Бальмера – совокупность линий в спектре атома водорода, соответствующих переходам со всех вышележащих уровней на уровень с n = 2. Только при n = 2 и m = 3, 4, 5, 6 излучаемые фотоны имеют длину волны Длины волн
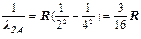 – зелено-голубая линия – зелено-голубая линия
Массы mф и импульсы рф данных фотонов можно найти по формулам:
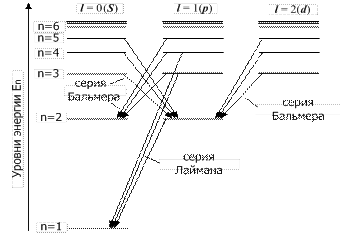
Схема некоторых переходов в атоме водорода приведена на рис. 1. Напомним смысл обозначений в этой схеме. Наряду с главным квантовым числом n состояние электрона в атоме характеризуется орбитальным квантовым числом l и магнитным квантовым числом ml . Состояния электрона с l = 0,1,2 обозначаются как s -, p - и d - состояния соответственно. Но уровни энергии электрона в атоме (а значит, и длины волн излучения) не зависят от чисел l, ml, а определяются только главным квантовым числом n. В квантовой механике доказывается, что возможны не любые переходы электронов в атоме, а лишь такие, при которых изменение орбитального квантового числа l соответствует правилу отбора
В соответствии с правилом (8), в первых двух сериях в спектре атома водорода разрешены переходы (см. рис. 1):
Рис. 1. Схема электронных переходов в атоме водорода
Описание установки
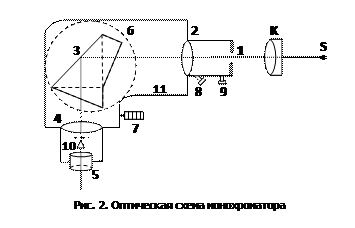
Схема экспериментальной установки представлена на рис. 2. 1. Свет от источника S проектируется конденсорной линзой K на входную щель 1, снабженную микрометрическим винтом 9, который позволяет открывать щель на нужную ширину. Рабочая ширина щели равна 0,02-0,03 мм. 2. Пройдя через щель, свет попадает на коллиматорный объектив 2, снабженный микрометрическим винтом 8, который позволяет смещать объектив относительно щели при фокусировке спектральных линий различных цветов и далее параллельным пучком проходит на сложную диспергирующую призму 3, установленную на поворотном столике.
3. Поворотный столик вращается вокруг вертикальной оси при помощи микрометрического винта 7 с отсчетным барабаном. На барабан нанесена винтовая дорожка с градусными делениями. Вдоль дорожки скользит указатель поворота барабана. При вращении барабана призма поворачивается, и в центре поля зрения появляются различные участки спектра. 4. Под углом 900 к падающему пучку света помещается зрительная труба монохроматора. Зрительная труба состоит из объектива 4 и окуляра 5. Объектив 4 дает изображение входной щели 1 в своей фокальной плоскости. В этой плоскости расположен указатель 10. Изображение рассматривается через окуляр 5, который может быть заменен выходной щелью, пропускающей одну из линий спектра (в этом случае прибор служит монохроматором). Вследствие явления дисперсии полихроматический свет, пройдя через призму, разделяется на монохроматические пучки, и в результате в окуляре 5 можно наблюдать ряд линий, каждая из которых представляет собой изображение входной щели, окрашенных в свой цвет. Поворачивая столик с призмой на различные углы относительно падающего пучка света, последовательно наблюдают в окуляре все эти линии. 5. Корпус 11 предохраняет прибор от повреждений и загрязнения. Источник света рекомендуется располагать на расстоянии 40-50 см от щели, а конденсор - на расстоянии 13-15 см от источника.
При подготовке прибора к работе особое внимание следует обращать на тщательную фокусировку для того, чтобы указатель 10 и спектральные линии имели четкие, ясные границы. Фокусировка производится в следующем порядке: перемещая окуляр 5, следует получить резкое изображение указателя 10. Для отсчета положения спектральной линии ее центр совмещают с острием указателя. Отсчет производится по делениям барабана. Для уменьшения погрешности ширину входной щели делают 0,02-0,03 мм по шкале микрометрического винта. Для наблюдения самых слабых линий в фиолетовой области щель нужно расширять до 0,05-0,06 мм. Глаз лучше замечает слабые линии в движении, поэтому при наблюдении полезно слегка поворачивать барабан в обе стороны от среднего положения.
Порядок выполнения работы
Задание 1. Градуировка спектроскопа по известным длинам волн спектра неона и ртути В качестве источника света взять неоновую лампу, установить ее на оптической скамье. После ее включения добиться четкой видимости спектральных линий в окуляре. 1. Медленно вращая барабан, следить за перемещением в поле зрения спектральных линий. Устанавливать барабан до упора в крайнее положение не желательно, так как при этом происходит сбивание шкалы. Когда центр первой красной линии совпадет с острием указателя, записать длину волны 2. Вращать барабан до совмещения центра второй линии с острием указателя и сделать аналогичные замеры. 3. Снять неоновую лампу, заменить ее ртутной лампой. Указания по включению ртутной лампы ДРШ приведены на рабочем месте. Во время работы ртутной лампы в ней развивается высокое давление, поэтому обращаться с ней следует осторожно. Допускается ее кратковременное включение от 3 до 5 минут! 4. Для ртутной лампы повторить действия в соответствии с пунктами 2 и 3, используя таблицу спектральных линий ртути на рабочем месте; эти данные занести в таблицу 1. 5. На миллиметровой бумаге построить градуировочный график спектроскопа, где по оси Х отложить деления барабана n
Таблица 1
Задание 2. Исследование серии Бальмера в видимой области спектра водорода 1. Установить трубку с водородом против входной щели и получить газовый разряд в ней с помощью высокочастотного генератора. Сначала найти наиболее интенсивную красную линию 2. С помощью градуировочного графика определить значения 3. Для каждого значения 4. Вычислить среднее значение постоянной Ридберга 5. Рассчитать теоретическое значение постоянной Ридберга 6. Рассчитать относительную погрешность
Задание 3. Определение массы и импульса фотонов, соответствующих линиям серии Бальмера Используя
Таблица 2
Техника безопасности При работе с ртутной лампой следует избегать попадания прямого света от лампы в глаза. Длительность непрерывной работы ртутной лампы 3-5 минут. Перед ее повторным включением необходима пауза 6 минут.
Контрольные вопросы 1. Что называют спектром испускания вещества? 2. Объясните происхождение линейчатых спектров в разреженных газах. 3. Объяснить устройство спектроскопа. 4. Какие квантовые числа характеризуют состояние электронов в атомах? Каков их физический смысл? 5. Сформулируйте правило отбора для орбитального квантового числа l. Какие переходы возможны в серии Бальмера атома водорода?
Рекомендуемая литература 1. Трофимова Т.И. Курс физики / Т.И. Трофимова. –М.: Высш. школа, 2001. 2. Савельев И.В. Курс общей физики. (т.3) / И.В. Савельев. – СПб.: Лань, 2006. 3. Детлаф А.А. Курс физики / А.А. Детлаф, Б.М. Яворский – М.: Академия, 2008.
Составители: Мардасова И.В., Пруцакова Н.В., Шполянский А.Я.
ИЗУЧЕНИЕ СПЕКТРА АТОМА ВОДОРОДА. МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЛАБОРАТОРНОЙ РАБОТЕ №4
(раздел «Атомная физика»)
Редактор Т.В. Колесникова ________________________________________________________ В печать 16.02.2012. Объем 0,75 усл.п.л. Офсет. Формат 60x84/16. Бумага тип №3. Заказ № Тираж 60 экз. Цена свободная ________________________________________________________ Издательский центр ДГТУ Адрес университета и полиграфического предприятия:

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
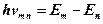 ,
, 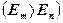
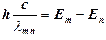 (1)
(1)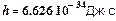 – постоянная Планка,
– постоянная Планка, 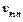 – частота излучения,
– частота излучения, 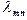 – длина волны,
– длина волны, 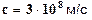 – скорость света в вакууме,
– скорость света в вакууме, 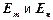 – энергии m - го иn - го состояний соответственно.
– энергии m - го иn - го состояний соответственно.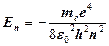 (n=1, 2, 3…), (2)
(n=1, 2, 3…), (2)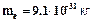 – масса электрона,
– масса электрона,  – заряд электрона,
– заряд электрона,  – электрическая постоянная. Формула (2) впервые получена Н. Бором. Для более сложных атомов эта формула несправедлива.
– электрическая постоянная. Формула (2) впервые получена Н. Бором. Для более сложных атомов эта формула несправедлива.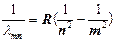 , (3)
, (3)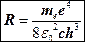 (4)
(4)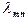 , попадающую в видимый участок спектра. При других значениях n и m фотоны соответствуют инфракрасному или ультрафиолетовому участкам спектра.
, попадающую в видимый участок спектра. При других значениях n и m фотоны соответствуют инфракрасному или ультрафиолетовому участкам спектра.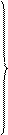
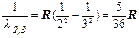 – красная линия
– красная линия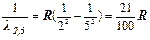 – фиолетово-синяя линия
– фиолетово-синяя линия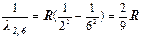 – фиолетовая линия
– фиолетовая линия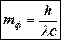 (6) и
(6) и 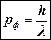 (7).
(7).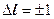 . (8)
. (8)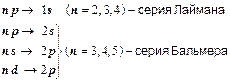
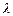 этой линии (по таблице спектральных линий неона на рабочем месте) и показания n на шкале барабана; эти данные занести в таблицу 1.
этой линии (по таблице спектральных линий неона на рабочем месте) и показания n на шкале барабана; эти данные занести в таблицу 1.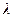 (в нм) соответствующих линий спектров неона и ртути. Этот график нужно использовать в дальнейшем для определения длин волн, излучаемых атомом водорода.
(в нм) соответствующих линий спектров неона и ртути. Этот график нужно использовать в дальнейшем для определения длин волн, излучаемых атомом водорода.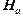 и установить острие указателя на данную линию, записать показания n шкалы барабана; эти данные занести в таблицу 2. Второй найти зелено-голубую линию
и установить острие указателя на данную линию, записать показания n шкалы барабана; эти данные занести в таблицу 2. Второй найти зелено-голубую линию 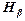 и произвести аналогичные замеры. В спектре водородной трубки наряду с линиями атомарного водорода наблюдается спектр молекулярного водорода; так, в промежутке между
и произвести аналогичные замеры. В спектре водородной трубки наряду с линиями атомарного водорода наблюдается спектр молекулярного водорода; так, в промежутке между 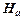 и
и 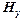 – фиолетово-синяя. Перед ней располагаются две слабые размазанные молекулярные полосы синего цвета. Четвертая линия
– фиолетово-синяя. Перед ней располагаются две слабые размазанные молекулярные полосы синего цвета. Четвертая линия  – фиолетовая, ее не всегда удается найти. Определить деления барабана, соответствующие линиям
– фиолетовая, ее не всегда удается найти. Определить деления барабана, соответствующие линиям  , занести их в таблицу 2.
, занести их в таблицу 2.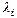 для каждой линии и занести их в таблицу 2.
для каждой линии и занести их в таблицу 2.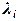 , найденного по графику, вычислить постоянную Ридберга
, найденного по графику, вычислить постоянную Ридберга  по формулам (5).
по формулам (5).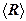 , ее абсолютную
, ее абсолютную 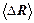 и относительную
и относительную 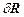 погрешности; данные занести в таблицу 2.
погрешности; данные занести в таблицу 2.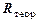 по формуле (4), занести в таблицу 2 и сравнить с
по формуле (4), занести в таблицу 2 и сравнить с 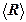 .
.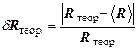 ; данные занести в таблицу 2.
; данные занести в таблицу 2.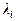 из таблицы 2, вычислить массу и импульс фотонов
из таблицы 2, вычислить массу и импульс фотонов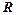
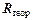
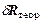
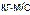
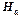
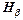
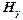

 344000, г. Ростов-на-Дону, пл. гагарина, 1.
344000, г. Ростов-на-Дону, пл. гагарина, 1.