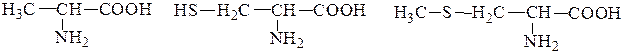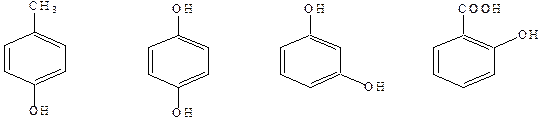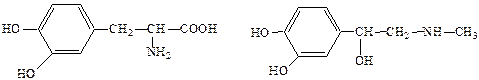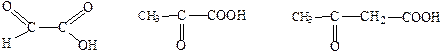|
|
Номенклатура органических соединенийII. Теоретическая часть 2.1. Введение.В настоящее время органическую химию определяют как химию углерода и его соединений — определение Бутлерова. Более точное определение было предложено Шорлеммером: органическая химия — это химия уг леводородов и их производных, причем в состав производных могут входить почти все элементы периодической системы. .
Классификация органических соединений Для описания структуры молекул органических соединений исполь- зуют различные химические формулы: эмпирические, молекулярные и структурные. Наиболее полную информацию о строении молекулы содер- жит структурная (графическая) формула, которая отражает природу ато- мов, входящих в состав молекулы, их число и последовательность связы- вания, а также тип связей между атомами.
H H H Обычно на практике наиболее часто употребляют полуструктурные формулы, т. е. часть связей не изображаются, а приводятся только те связи, которые необходимы для однозначного описания строения молекулы: СН3 – СН2 – СН2 –СН3 СН3 – СН – СН2 –СН3 | NH2
|| O
Каждый период истории развития органической химии отмечен по- пытками химиков каким-то образом привести разнообразные химические соединения В основе современной классификации органических соединений лежит теория строения А.М. Бутлерова, согласно которой каждое индивидуальное вещество можно описать только одной химической формулой (рисунки 1 и 2). в единую систему (теория типов, радикалов и т. д.).
Циклические
Карбоциклические Гетероциклические
Алициклические Ароматические
Рисунок 1 — Классификация органических соединений
Алкенины Алкадиены
Алкены
Алкины
Алкадиены
Полиены
Непредельные углеводороды Кумулированные
сопряженные изолированные
Ациклические углеводороды
Предельные углеводороды
Рисунок 2 — Схема классификации ациклических соединений
Предельные или насыщенные углеводороды (алканы, парафины) содер- жат только простые углерод-углеродные связи, все остальные валентности атомов углерода в их молекулах «израсходованы» на связи с водородными атомами. Общая формула СnН2n+2. Родоначальник ряда — метан СН4. Непредельные или ненасыщенные углеводороды имеют кратные (двойные или тройные) углерод — углеродные связи. Алкены (олефины, этиленовые углеводороды) содержат одну двойную связь. Общая формула СnН2n.Родоначальник ряда — этилен СН2 = СН2. Алкины (ацетиленовые углеводороды) имеют тройную связь. Общая формула СnН2n-2. Родоначальник ряда — ацетилен СН≡СН. Алкадиены (диолефины, диеновые углеводороды) содержат две двой- ные связи. Общая формула такая же как у алкинов СnН2n-2, т.е. алкины и алкадиены изомерны друг другу. Различают: 1) алкадиены с изолированными двойными связями, например, Н2 С = СН – СН2 – СН = СН2пентадиен-1,4; 2) алкадиены с сопряженными двойными связями, например, Н2 С = СН – СН = СН – СН3пентадиен-1,3; 3) алкадиены с кумулированными двойными связями, например, Н2 С = С = СН – СН2 – СН3пентадиен-1,2; 4) алкенины –соединения с одной двойной и одной тройной связями Н2 С = СН – С ≡ СНбутен-1-ин-3; 5) алкадиины – соединения с двумя тройными связями НС ≡ С – С ≡ СНбутадиин-1,3; 6) полиены (полиолефины) — соединения со многими двойными связями Н2С = СН – СН = СН – СН = СН – СН3гептатриен-1,3,5.
Алициклические углеводороды
Циклоалкадиены — циклические соединения, содержащие две двой- ные связи. Общая формула — СnН2n-4.
Алициклические соединения могут содержать один, два и более цик- лов. Бициклические соединения в зависимости от способа соединения циклов могут быть:
спиро-[2,5]-октан бицикло-[4,2,0]-октан бицикло-[3,2,1]-октан
Ароматические соединения (арены) — группа карбоциклов, характе- ризующихся наличием ароматической системы. Ароматические соедине- ния бывают двух видов: • бензоидные ароматические соединения — обязательной составной ча- стью молекулы является бензольное ядро; • небензоидные ароматические соединения — структуры, отвечающие тре- бованиям ароматичности, но лишенные шестичленных ароматических колец. Функциональная группа – структурный фрагмент молекулы, опреде- ляющий ее химические свойства.
R -Hal R -OH R -SH R - O - R R - SO3H галог ен производные спирты, фенолы тиолы простые эфиры сульфо кислоты O R - C
O
OH
альдег иды кетоны
карбоновые кислоты
R - C
R - C
R - C O
соли карбоновых кислот
сложные эфиры
амиды
R - C
R - C
R - C
R
галог ен анг идриды
анг идриды карбоновых кислот
оксимы
R - C
гидразиды кислот R'
R - NO2
нитросоединения R - NH2
R - NH - R'
первичные амины
вторичные амины
третичные амины
R - CN
R - NH - NH2 R - N2 R - N = N - R '
нитрилы г идразины диазосоединения
азосоединения
Номенклатура органических соединений Номенклатура — это совокупность названий веществ, их групп и классов, а также система правил, обеспечивающих однозначную связь на- званий и формул, выражающих строение молекул. Номенклатура органических соединений складывалась на протяжении всего периода развития органической химии и становления ее как науки. Первая номенклатура — тривиальная. Названия соединений случай- ные, обусловлены различными обстоятельствами (в основе лежат различ- ные отличительные признаки).
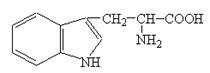
Источники выделения Например, винная кислота выделена из винного камня со дна винных бочек. Аналогично — муравьиная кислота, янтарная кислота, молочная кислота, лимонная кислота и др. Тирозин (от греч.tirosin) — сыр.
Отличительные свойства Глицин (от греч. glykos) — сладкий. Лейцин (от греч. leykas) — белый. Акролеин (от лат. acris) — жгучий.
Способы выделения (получения) Пировиноградная кислота (ПВК) получена пиролизом винной кислоты. Гидрохинон – восстановлением бензохинона. Область применения Витамин РР (никотинамид) — предупреждает пелагру. Кордиамин — препарат, применяемый как сердечное средство. Тривиальная номенклатура не имеет никакой научной основы, однако многие названия прочно укоренились и широко используются, особенно в химии биологически-активных соединений. Затем появляется рациональная номенклатура, согласно которой все соединения в данном гомологическом ряду рассматриваются как произ- водные простейшего соединения для данного гомологического ряда. СН3 | Н3С – С – СН3 тетраметилметан | СН3
CH3 / Н3С – С Н2– СН = С диметилэтилэтилен \ CH3 Рациональной номенклатурой в настоящее время пользуются редко, однако основные принципы нашли отражение и в современных номенкла- турных правилах. Радикально-функциональная номенклатура используется вместо ра- циональной для названий моно- и бифункциональных соединений некото- рых классов природных соединений (терпены, стероиды, алкалоиды и дру- гие). В названии старшей характеристической группы не применяются суффиксы, называют радикал и основной класс соединений. O // Н3С – С ацетилхлорид \ Сl
Н5С2 – CN этилцианид
Н3С – СН – СН2 – ОН изобутиловый спирт | CH3 Н2С = СН – Cl винилхлорид
Н3С – С – С6Н5 метилфенилкетон || О Н3С – О – С2Н5 метилэтиловый эфир В настоящее время признанной во всем мире является номенклатура IUPAC(International Union of Pure and Applied Chemistry — Международ- ный союз чистой и прикладной химии). Ее еще называют международной, систематической, женевской (так как основы заложены в 1892 г. на меж- дународном конгрессе химиков в г. Женеве), льежской (усовершенствова- на и дополнена в 1930 г. в г. Льеже). Название IUPACноменклатура полу- чила на ХIХ конгрессе Международного союза чистой и прикладной хи- мии в 1957 г.
ОБЩАЯ СХЕМА СОСТАВЛЕНИЯ НАЗВАНИЙ
–OR – алкокси –SR – алкилтио –SC6H5 – арилтио –NO2 – нитро –NO – нитрозо –N=N– – азо
Рассмотрим несколько примеров: 2 1 H2N – CH2 – CH2 – OH 2-аминоэтанол-1 (коламин) – биогенный амин 6 5 4 3 2 1 Н2C – CH2 – CH2 – CH2 – CH – COOH | | NH2 NH2 2,6-диаминогексановая кислота (лизин) 4 3 2 1 Н2C – CH2 – CH – COOH 2-амино-4-метилтиобутановая | | кислота (метионин) S-CH3 NH2
OH | НООС –СН2– С – СН2 –СООН | 3-гидрокси-3-карбоксипентандиовая COOH кислота (лимонная кислота) Таблица 1 — Важнейшие функциональные группы, расположенные в порядке убывания старшинства
2.4.Составление названия органического соединения по заместительной номенклатуре производят в последовательности: 1. Определяют старшую характеристическую группу (с учетом относительного старшинства) и родоначальную структуру соединения (главная цепь атомов углерода в ациклических соединениях и основную циклическую структуру в карбо- и гетероциклических структурах – а)максимальное число х.г., обозначаемых и префиксами и суффиксами; б)максимальное число кратных связей; в) максимальная длина цепи атомов углерода; г) максимальное число х.г., обозначаемых только префиксами. Каждый последующий критерий используют в том случае, если предыдущий не приводит к однозначному выводу). 2. Нумеруют атомы родоначальной структуры так, чтобы старшая х.г. получила наименьший номер (или сумма номеров заместителей была наименьшей).В гетероцикле начало нумерации определяет гетероатом. 3.Называют родоначальную структуру, обозначая старшую характеристическую группу суффиксом. Степень насыщенности родоначальной структуры отражают в ее названии суффиксами-ан, -ен-, ин. 4. Называют заместители, обозначаемые префиксами, в едином алфавитном порядке. Положение каждого заместителя и каждой кратной связи указывают цифрами, соответствующими номеру атома С, с которым связан заместитель. Рассмотрим несколько примеров: 2 1 H2N – CH2 – CH2 – OH 2-аминоэтанол-1 (коламин) – биогенный амин 6 5 4 3 2 1 Н2C – CH2 – CH2 – CH2 – CH – COOH | | NH2 NH2 2,6-диаминогексановая кислота (лизин) 4 3 2 1 Н2C – CH2 – CH – COOH 2-амино-4-метилтиобутановая | | кислота (метионин) S-CH3 NH2
OH | НООС –СН2– С – СН2 –СООН | 3-гидрокси-3-карбоксипентандиовая COOH кислота (лимонная кислота)
III. Обучающие упражнения Большинство природных соединений и фармацевтических препаратов включают в свою структуру по меньшей мере одну или несколько функциональных групп. Гетерофункциональность – это признак природных соединений, участвующих в обеспечении жизнедеятельности. К гетерофункциональным соединениям относя гирокси-, оксо-, аминокислоты, аминоспирты, углеводы и др. Алгоритм построения названия гетерофункционального соединения 1. выбирают старшую характеристическую группу, используя шкалу старшинства; 2. определяют родоначальную структуру и нумеруют её так, чтобы старшая характеристическая группа получила наименьший локант (учитывается правило наименьших локантов); 3. определяют заместители, называют их префиксами в алфавитном порядке, с указанием цифры, соответствующей положению заместителя в родоначальной структуре; 4. называют родоначальную структуру, присоединяя суффикс старшей характеристической группы. Задание 1. Назвать по систематической номенклатуре следующие соединения:
Задание 2. Привести структурные формулы и систематические названия изомеров γ-аминомасляной кислоты (ГАМК).
Задание 3. Указать характеристические группы. Назвать по систематической номенклатуре: L-карнитин
3-гидрокси-4-N,N,N,-триметиламинобутановая кислота
V. Задания для самостоятельной работы Задание 1. Назвать по систематической номенклатуре следующие соединения:
этаноламин холин
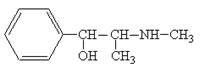
тирозин норадреналин
ДОФА адреналин
глиоксалевая кислота пировиноградная кислота ацетоуксусная кислота
Задание 2. Привести формулы следующих соединений по их названию: 1) напишите формулу ментола (2-изопропил-5-метилциклогексанол-1), который входит в состав препарата валидол. 2) 8-гидроксихинолина, и продукта синтеза на его основе препарата 5-НОК (8-гидрокси-5-нитрохинолина). 3) антидота, использующегося при отравлениях мышьяком (2,3-димеркаптопропанол) (БАЛ). 4) аминокислоты серина (2-амино-З-гидроксипропановой кислоты); 5) пиридоксин (витамин В6) представляет собой производное пиридина. Приведите структурную формулу витамин В6 по его систематическому названию: З-гидрокси-4,5-дигидроксиметил-2-метилпиридин. IV. Подведение итогов занятия. Домашнее задание: 1) Выучить основы классификации и номенклатуры органических соединений 2) Разобрать обучающие упражнения 3) Выполнить задания для самостоятельной работы. 4) Подготовиться к выполнению САРС или тестового задания по изученной теме.
Основная литература 1. Тюкавкина Н.А., Бауков Ю.И. , Зурабян С.Э. .Биоорганическая химия. Учебник. М.: ГЭОТАР-Медиа. 2010 – 416 с. 2. Под редакцией Тюкавкиной Н.А. Биоорганическая химия. Руководство к практическим занятиям, М.:ГЭОТАР-Медиа,2009 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

 H H H
H H H





 NH2
NH2 CH3 -C - CH3
CH3 -C - CH3 ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ Ациклические
Ациклические В свою очередь, схема классификации ациклических соединений име- ет вид:
В свою очередь, схема классификации ациклических соединений име- ет вид: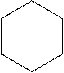 Циклоалканы (циклопарафины, полиметилены, цикланы) — циклические соединения, содержащие только простые одинарные связи. Общая формула — СnН2n.
Циклоалканы (циклопарафины, полиметилены, цикланы) — циклические соединения, содержащие только простые одинарные связи. Общая формула — СnН2n.

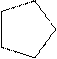 циклопропан циклобутан циклопентан циклогексан
циклопропан циклобутан циклопентан циклогексан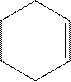 Циклоалкены (циклоолефины, циклены) — циклические соединения, которые содержат двойную связь. Общая формула — СnН2n-2.
Циклоалкены (циклоолефины, циклены) — циклические соединения, которые содержат двойную связь. Общая формула — СnН2n-2.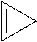 циклопропен циклогексен
циклопропен циклогексен
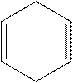 циклопентадиен-1,3 циклогексадиен-1,4
циклопентадиен-1,3 циклогексадиен-1,4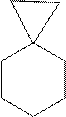

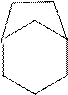 спирановые конденсированные мостиковые
спирановые конденсированные мостиковые
 H
H R - C - R'
R - C - R'
 O R - C
O R - C
 OMe O
OMe O
 OR O NH2
OR O NH2 O
O O
O
 Cl O
Cl O
 O O
O O
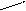 C = N - OH
C = N - OH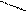 NH - NH2
NH - NH2 R - N - R' R"
R - N - R' R"