Критическое давление и скорость. Сопло Лаваля.
Если перемещение газа по каналу происходит его расширение с уменьшением давления и увеличением скорости, то такой канал называется соплом.
Если в канале происходит сжатие рабочего тела с увеличением его давления и уменьшением скорости, то такой канал называют диффузором.
В каналах при небольшой разности давлений газа и внешней среды скорость течения рабочего тела достаточно большая. В большинстве случаев длина канала небольшая и процесс теплообмена между стенкой и газом незначителен, поэтому процесс истечения газа можно считать адиабатным.
Скорость истечения (на выходе канала) определяется из уравнения:
w = w2 = v 2(h1 – h2) . (5.6)
или
w = v 2Ö/(g - 1)·P1·х 1 [1 – (P2/P1)(g-1)/g]. (5.7)
Массовый секундный расход газа, [кг/с]:
m = f·w/х 2 , (5.8)
где: f – площадь сечения канала на выходе.
Так как процесс истечения адиабатный, то:
m = f·Ö 2g/(g - 1)·P1/х 1·[(P2/P1)2/g – (P2/P1)(g+1)/g]. (5.9)
Массовый секундный расход идеального газа зависит от площади выходного канала, начального состояния газа и степени его расширения.
Критическим давлением называется такое давление на выходном сечении канала, при котором достигается максимальный расход газа и определяется следующим выражением:
PК = P2 = bК·P1 , (5.10)
где: PК = (2/(g + 1))г/(г-1) .
для одноатомных газов: g =1,66 q bК = 0,49 ;
для двухатомных газов: g =1,4 q bК = 0,528 ;
для трехатомных газов: g =1,3 q bК = 0,546 .
Критической скоростью называется скорость газа в выходном сечении канала, при давлении равном или меньшем критического - PК.
wК = Ö 2(g/(g + 1))·P1·х 1 . (5.11)
Критическая скорость зависит при истечении идеального газа только от начальных параметров, его природы и равна скорости звука газа (а) при критических параметрах.
wК = а = Ö g·PК·хК . (5.12)
Комбинированное сопло Лаваля предназначено для использования больших перепадов давления и для порлучения скоростей истечения, превышающих критическую или скорость звука. Сопло Лаваля состоит из короткого суживающегося участка и расширяющейсяя конической насадки (Рис.5.1). Опыты показывают, что угол конусности расширяющейся части должен быть равен a = 8-12о. При больших углах наблюдается отрыв струи от стенок канала.
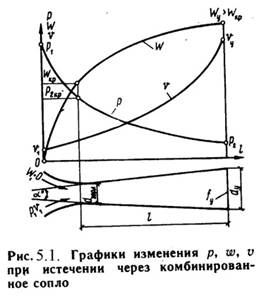
Скорость истечения и секундный расход идеального газа определяются по формулам (5.7) и (5.9).
Длину расширяющейся части сопла можно определить по уравнению:
l = (D – d) / 2·tg(j/2) , (5.13)
где: j - угол конусности сопла;
D - диаметр выходного отверстия;
d - диаметр сопла в минимальном сечении.
Дросселирование.
Дросселированием называется явление, при котором пар или газ переходит с высого давления на низкое без совершения внешней работы и без подвода или отвода теплоты. Такое явление происходит в трубопроводе, где имеется место сужения проходного канала (Рис.5.2). При таком сужении, вследствие сопротивлений, давление за местом сужения - Р2, всегда меньше давления перед ним – Р1.
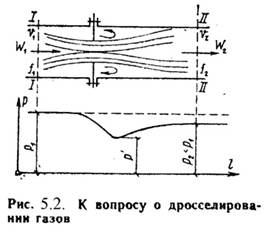
Любой кран, вентиль, задвижка, клапан и прочие местные сопротивления, уменьшающие проходное сечение трубопровода, вызывают дросселирования газа или пара, следовательно падения давления. В большинстве случаев это явление приносит безусловный вред. Но иногда оно является необходим и создается искусственно (регулирование паровых двигателей, в холодильных установках, в приборах для измерения расхода газа и т.д.).
При прохождении газа через отверстие, кинетическая энергия газа и его скорость в узком сечении возрастают, что сопровождается падением температуры и давления.
Газ, протекая через отверстие, приходит в вихревое движение. Часть его кинетической энергии затрачивается на образование этих вихрей и превращается в теплоту. Кроме того, в теплоту превращается и работа, затраченная на преодоление сопротивлений (трение). Вся эта теплота воспринимается газом, в результате чего температура его изменяется (уменьшается или увеличивается).
В отверстие скорость газа увеличивается. За отверстием газ опять течет по полному сечению и скорость его вновь понижается. А давление увеличивается, но до начального значения оно не поднимается; некоторое изменение скорости произойдет в связи с увеличением удельного объема газа от уменьшения давления.
Дросселирование является необратимым процессом, при которм происходит увеличение энтропии и уменьшение работоспособности рабочего тела.
Уравнением процесса дросселирования является следующее уравнение:
i1 = i2 . (5.14)
Это равенство показывает, что энтальпия в результате дросселирования не изменяется и справедливо только для сечений, достаточно удаленных от сужения.
Для идеальных газов энтальпия газа является однозначной функцией температуры. Отсюда следует, что при дросселировании идеального газа его температура не изменяется (Т1 = Т2).
При дросселировании реальных газов энтальпия газа остается постоянной, энтропия и объем увеличиваются, давление падает, а температура изменяется (увеличивается, уменьшается или остется неизменной).
Изменение температуры жидкостей и реальных газов при дросселировании называется эффектом Джоуля-Томсона. Для идеального газа эффект Джоуля-Томсона равен нулю. Различают дифференциальный температурный эффект, когда давление и температура изменяются на бесконечно малую величину, и интегральный температурный эффект, при котором давление и температура изменяются на конечную величину.
Дифференциальный температурный эффект обозначается - б:
a = (¶T/¶P)i . (5.15)
Интегральный температурный эффект определяется из следующего уравнения:
DT = T2 – T1 = ò [T·(¶n/¶T)p – n] / cp dP . (5.16)
Для реальных газов DT¹0 и может иметь положительный или отрицательный знак.
Состояние газа, при котором температурный эффект меняет свой знак, называется точкой инверсии, а температура, соответствующая этой точке, называется температурой инверсии - Тинв.
Тинв = n·(¶Т/j¶ n)p . (5.17)
Тема 6. Реальные газы. Водяной пар. Влажный воздух.
Свойства реальных газов.
Реальные газы отличаются от идеальных газов тем, что молекулы этих газов имеют объемы и связаны между собой силами взаимодействия, которые уменьшаются с увеличением расстояния между молекулами. При практических расчетах различных свойств реальных газов наряду с уравнением состояния применяется отношение P·n/(R·T)=c, которая называется коэффициентом сжимаемости.
Так как для идеальных газов при любых условиях P·n = R·T, то для этих газов с = 1. Тогда величина коэффициента сжимаемости выражает отклонение свойств реального газа от свойств идеального. Величина с для реальных газов в зависимости от давления и температуры может принимать значения больше или меньше единицы и только при малых давлениях и высоких температурах она практически равна единице. Тогда реальные газы можно рассматривать как идеальные.
В связи с отличием свойств реального газа от свойств идеального газа нужно иметь новые уравнения состояния, которые связывали бы значения P, х, T и давали бы возможность рассчитывать некоторые свойства газов для разных условий. Были предложены многочисленное число различных уравнений состояния реальных газов, но ни одно из них не решает проблему для общего случая. Развитие кинетической теории газов, позволило установит точное уравнение состояния реальных газов в виде:
P·n = R·[1 - Sn /(n + 1)·Bn / nn]. (6.1)
Bn – вириальные коэффициенты, выражаются через потенциальные энергию взаимодействия молекул данного газа и температуру Т.
Однако это уравнение в общем виде не может быть использовано для непосредственных расчетов реальных газов. Для отдельных частных случаях получены расчетные уравнения того или иного реального газа. Из-за сложности вычисления вириальных коэффициентов обычно ограничиваются расчетом первых двух коэффициентов. Тогда расчетное уравнение имеет вид:
P·n = R·(1 – А/n - B / n2), (6.2)
где А и В - первый и второй вириальные коэффициенты, являющиеся функцией только температуры.
При расчете свойств многих реальных газов уравнения такого типа получили большое распространение.
Не нашли, что искали? Воспользуйтесь поиском по сайту:
©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|



