
|
|
Общие сведенья об атомах и атомных ядрах.
В ядре сосредоточена практически вся масса атома (99,95%). При Рис.1 обычных условиях атом является электрически нейтральным, так как положительный заряд ядра компенсируется отрицательным зарядом электронов. Размеры атомов, так же как и их масса, чрезвычайно малы, и составляют около 1 нм (1·10-9 м). Электроны очень лёгкие, почти невесомые, имеют отрицательный заряд (заряд электрона условно равен -1, соответствуетэлементарному заряду qe= Атомное ядро любого химического элемента состоит из положительно заряженных протонов и не имеющих электрического заряда нейтронов. Заряд протона по абсолютной величине равен заряду электрона. Протон и нейтрон являются двумя зарядовыми состояниями ядерной частицы, которая называется нуклоном. Внутри ядра протоны и нейтроны способны к взаимному превращению, однако количество протонов и нейтронов в ядре всегда величина постоянная для данного нуклида и является его важной характеристикой. Массовым числом А называется общее число нуклонов в ядре. Массовые числа нейтрона и протона одинаковы и равны 1 а.е.м.. Число протонов в ядре равно числу электронов и называется зарядовым числом Z, оно совпадает с порядковым номером (атомным номером) атома данного химического элемента в периодической системе Менделеева: №пор= Z . Чтобы определить число нейтронов N надо от массового числа A отнять атомный номер Z (или зарядовое число): N = A − Z. Нуклиды обозначаются в общем виде следующим образом: Электроны, движущиеся вокруг ядра, сгруппированы в электронные слои, каждый из которых содержит электроны с близкими значениями энергии. Ядра элементов весьма устойчивы. Это значит, что кроме кулоновских сил отталкивания между протонами в ядре действуют и значительные силы притяжения, которые называют ядерными. Ядерные силы имеют следующие основные особенности: 1. Они действуют только на очень коротких расстояниях порядка размера самого ядра и за его пределами равны нулю. 2. Ядерные силы в сотни и тысячи раз превышают все другие известные в природе взаимодействия. 3. Они действуют независимо от заряда нуклона. 4. Они имеют свойства насыщения: каждый нуклон взаимодействует только с соседним с ним нуклонами, и при увеличении количества нуклонов в ядре, ядерные силы не возрастают. 5. Ядерные силы обладают особой обменной природой, не имеющей аналогий в классической физике. Согласно теории, нуклоны в ядре удерживаются вместе путем непрерывного обмена особыми элементарными частицами, которые называются квантами ядерного поля или Устойчивость атомных ядер, изотопы. Химические свойства любого элемента не зависят от массового числа; т. к. они определяются строением электронных оболочек атома (следовательно, и Z). С другой стороны, массовое число имеет решающее значение для ядерной стабильности радиоактивных свойств атома. Для стабильных ядер отношение количества нейтронов N к количеству протонов Z равно единице: N / Z = 1, ядра для которых N / Z больше или равно 1,5 являются нестабильными. Так, например, для изотопа Для радиоактивных изотопов элементов, находящихся в начале и середине таблицы Менделеева, такой закономерности не обнаружено. Вместе с тем, для таких достаточно широко распространенных радионуклидов как Изотопы–атомы, которые имеют одинаковый атомный номер Z (одинаковый заряд ядер) и разные массовые числа. Они идентичны по химическим свойствам, но различаются по характеру радиоактивности. В таблице Менделеева более 100 химических элементов. Почти каждый из них представлен смесью стабильных и радиоактивных атомов, которые называют изотопами данного элемента. Известно около 2000 изотопов, из которых около 300 - стабильных. Например, углерод встречается в виде смеси трех изотопов - Изотопы имеют одинаковый символ и определяются общим названием элемента с добавлением к нему массового числа. Например, углерод – 12, калий – 40, уран – 235 и т.д. Радиоактивные изотопы обычно называют радионуклидами. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 В 1911 году, английский учёный Эрнест Резерфорд предложил "планетарную" модель атома, согласно которой в центре атома расположено крохотное, но очень плотное ядро, в котором сосредоточена почти вся масса атома, а электроны вращаются вокруг него по определённым орбитам, как планеты вокруг Солнца (рис.1). Именно этой моделью пользуются до сегодняшнего дня.
В 1911 году, английский учёный Эрнест Резерфорд предложил "планетарную" модель атома, согласно которой в центре атома расположено крохотное, но очень плотное ядро, в котором сосредоточена почти вся масса атома, а электроны вращаются вокруг него по определённым орбитам, как планеты вокруг Солнца (рис.1). Именно этой моделью пользуются до сегодняшнего дня. ).
). или
или  , где Х – символ химического элемента, А – массовое число, Z - зарядовое число или атомный номер. Например,
, где Х – символ химического элемента, А – массовое число, Z - зарядовое число или атомный номер. Например,  ,
,  ,
,  и т.д.
и т.д. -мезонами. Время обмена составляет~10–23 с.
-мезонами. Время обмена составляет~10–23 с. 
 отношение
отношение  =1,271, а для изотопа
=1,271, а для изотопа  данное отношение уже равно 1,598. Такая перегруженность ядер нейтронами и возрастание сил кулоновского отталкивания приводит к потере прочности ядра и поэтому все известные изотопы химических элементов с Z
данное отношение уже равно 1,598. Такая перегруженность ядер нейтронами и возрастание сил кулоновского отталкивания приводит к потере прочности ядра и поэтому все известные изотопы химических элементов с Z  являются радиоактивными.
являются радиоактивными.
 ,
,  ,
,  ,
,  ,
,  и др. соотношение нейтронов к протонам колеблется в пределах от 1,1 для
и др. соотношение нейтронов к протонам колеблется в пределах от 1,1 для  до 2 для
до 2 для 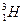 .
. ,
,  , ядра которых содержат 6 протонов и, соответственно, 6, 7 и 8 нейтронов.
, ядра которых содержат 6 протонов и, соответственно, 6, 7 и 8 нейтронов.