
|
|
Основные газовые процессы. Изохорный процессОсновными термодинамическими процессами являются: 1) процесс сообщения или отнятия теплоты при постоянном объеме газа (V=const) – изохорный процесс; 2) процесс сообщения или отнятия теплоты при постоянном давлении (P=const) – изобарный процесс; 3) процесс сообщения или отнятия теплоты при постоянной температуре (T=const) – изотермический процесс; 4) процесс без сообщения или отнятия теплоты извне (dq=0) - адиабатный процесс; 5) процесс, в котором изменение параметров подчиняется уравнению
где m - величина, постоянная для данного процесса, - политропный процесс. В изохорном процессе зависимость между начальными и конечными параметрами определяется следующей зависимостью
Изменение внутренней энергии
Если в процессе участвует
Задачи 7.1. Газ при давлении Р1=1МПа и температуре t1=20 ОС нагревается при постоянном объеме до t2=300 ОС. Найти конечное давление газа. Ответ: Р2=1.956 МПа. 7.2. В закрытом сосуде емкостью V=0.3 м3 содержится 2.75 кг воздуха при давлении Р1=0.8 МПа и температуре t1=25 ОС. Определить давление и удельный объем после охлаждения воздуха до 0 ОС. Ответ: Р2=0.732 МПа, v2=0.109 м3/кг. 7.3. В закрытом сосуде заключен газ при разрежении Р1=6667 Па и температуре t1=70 ОС. Показание барометра - 101325 Па. До какой температуры нужно охладить газ, чтобы разрежение стало Р2=13 332 Па? Решение: Так как процесс происходит при V =const , то согласно формуле (7.1) (101 325-6667)/(101 325-13332)=(273+70)/T2.
Отсюда Т2=87993*343/94658=318.8 K; t2=45.8°С. Ответ: t2=45.8 °С 7.4.До какой температуры t2 нужно нагреть газ при V=const , если начальное давление газа P1=0.2 МПа и температура t1=20 °С, а конечное давление P2=0.5 МПа. Ответ: До t2=459.5 °С. 7.5. В закрытом сосуде емкостью V=0.6 м3 содержится воздух при давлении р1=0.5 МПа и температуре t1=20 °С. В результате охлаждения сосуда воздух, содержащийся в нем, теряет 105 кДж. Принимая теплоемкость воздуха постоянной, определить, какое давление и какая температура устанавливаются после этого в сосуде. Решение: Пользуясь уравнением состояния, находим массу воздуха в сосуде M=РV/RT=0.5∙106∙0.6/287∙293=3.57 кг. Количество теплоты, отводимой от воздуха в процессе, определяется уравнением Q=Mcvm(t2-t1) откуда t2=Q/Mcvm+t1= -105/3.57∙0.723+20= -40.7+20= -20.7 °С. Значение сvm=0.723 получено из выражения cvm=mcvm/m=20.93/28.96 (для двухатомных газов). Из соотношения параметров в изохорном процессе имеем Р2=Р1∙Т2/Т1=0.5∙(273-20.7)/293=0.43 МПа. Ответ: Р2=0.43 МПа 7.6. В закрытом сосуде емкостью V=0.5 м3 содержится двуокись углерода при р1=0.6 МПа и температуре t1=527 °С. Как изменится давление газа , если от него отнять 420 кДж? Принять зависимость С=f(t) линейной. Ответ: р2=0.42 МПа. 7.7. Сосуд емкостью 90 л содержит воздух при давлении 0.8 МПа и температуре 30 °С. Определить количество теплоты, которое необходимо сообщить воздуху, чтобы повысить его давление при V=const до 1.6 МПа. Принять зависимость с=f(t) нелинейной. Решение: Из соотношения параметров изохорного процесса получим Т2=Т1∙P2/P1=303∙1.6/0.8=606 К, t2=606-273=333°С. По уравнению qv=cvm2t2-cvm1t1. Пользуясь табл. 4.2,4.3 , находим сvm1=0.7173 кДж/кг К ; cvm2=0.7351 кДж/кг К.. Следовательно, qv=0.7351∙333-0.7173∙30=223.2 кДж/кг. Массу воздуха, находящегося в резервуаре, определяем из уравнения M=p1V1/RT1=0.8∙106∙0.09/287∙303=0.8278 кг, а сообщенное ему количество теплоты Qv=0.8278∙223.2=184.8 кДж. 7.8. До какой температуры нужно охладить 0.8 м3 воздуха с начальным давлением 0.3 МПа и температурой 15°С , чтобы давление при постоянном объеме понизилось до 0.1 МПа? Какое количество теплоты нужно для этого отвести? Теплоемкость воздуха принять постоянной. Отв. До t2= -177°С; Q=- 402 кДж. Изобарный процесс Процесс сообщения или отнятия теплоты при постоянном давлении называется изобарным (P=const) Зависимость между начальными и конечными параметрами процесса
Работа 1 кг газа
или
Для М кг газа
или
Если в процессе
Задачи 8.1. Какое количество теплоты необходимо затратить , чтобы нагреть 2 м3 воздуха при постоянном избыточном давлении р=0.2 МПа от t1=100°С до t2=500°С? Какую работу при этом совершит воздух? Давление атмосферы принять равным 101 325 Па. Решение: Согласно уравнению qp=cpm2t2-cpm1t1. cpm1=1.0061 кДж/кг К; cpm2=1.0387 кДж/кг К. Следовательно, qp=1.0387∙500-1.0061∙100=418.7 кДж/кг. Массу воздуха определяем из характеристического уравнения M=РV/RT=(0.2+0.1013)106∙2/287∙373=5.63 кг. Таким образом , Qp=Mqp=5.63∙418.7=2357 кДж. Количество теплоты можно получить не только по массе воздуха , но и по его объему. В этом случае уравнение следует написать так: qp=с’pm2t2-c’pm1t1. Пользуясь табл. 4.2, получаем c’pm1=(c’pm)0100=1.3004 кДж/м3 К; c’pm2=(c’pm)0500=1.3427 кДж/м3 К. Тогда qp=1.3427∙500-1.3004∙100=541.4 кДж/м3. Объем воздуха должен быть приведен к нормальным условиям. Согласно уравнению Vн=pVTн/Tpн=0.3013∙2∙273/373∙0.1013=4.35 м2. Таким образом, Qp=qpVн=541.4∙4.35=2356 кДж. Работа газа по уравнению L=MR(t2-t1)=5.63∙287∙400=646.3 кДж. 8.2. Определить количество теплоты , необходимое для нагревания 2000 м3 воздуха при постоянном давлении р=0.5 МПа от t1=150°С до t2=600°С. Зависимость теплоемкости от температуры считать нелинейной. Ответ: Qр=3937 МДж. 8.3. В установке воздушного отопления внешний воздух при t1=-15°С нагревается в калорифере при р=const до 60°С. Какое количество теплоты надо затратить для нагревания 1000 м3 наружного воздуха? Теплоемкость воздуха считать постоянной. Давление воздуха принять равным 101 325 Па. Отв. 103 МДж. 8.4. В цилиндре находится воздух при давлении р=0.5 МПа и температуре t1=400°С. От воздуха отнимается теплота при постоянном давлении таким образом, что в конце процесса устанавливается температура t2=0°С. Объем цилиндра , в котором находится воздух , равен 400 л. Определить количество отнятой теплоты, конечный объем, изменение внутренней энергии и совершенную работу сжатия. Зависимость теплоемкости от температуры считать нелинейной.
Решение: Количество отнятой теплоты по формуле Qp=Vнc”pm(t2-t1). Объем воздуха при нормальных условиях определим из выражения Vн=pVTн/pнT=0.5∙0.4∙273/0.1013∙673=0.8 м3. По табл. 4.2, 4.3 находим c’pm=1.3289 кДж/м3 К. Следовательно, Qp=0.8∙1.3289(0-400)=- 425кДж. Это же количество теплоты можно вычислить не только по объему воздуха , но и по его массе: Qp=Mcpm(t2-t1). Массу воздуха определяем из характеристического уравнения M=Р1V1/RT1=0.5∙106∙0.4/287∙673=1.035 кг. Из табл. 4.2 находим cpm=1.0283 кДж/кг К. Следовательно, Qp=1.035∙1.0283(0-400)=-425 кДж. Конечный объем получим из уравнения (10.4) V2=V1T2/T1=0.4∙273/673=0.1622 м3. Изменение внутренней энергии DU=Vнc’vm(t2-t1). Пользуясь табл. 4.2, находим c’vm=0.9579 кДж/м3 К. Следовательно, DU=0.8∙0.9579(0-400)=-306.5 кДж. Работа, затраченная на сжатие, по формуле (8.4) L=Р(V2-V1)=0.5∙106(0.1622-0.4)=-118.9 кДж. 8.5. Для использования отходящих газов двигателя мощностью N=2500 кВт установлен подогреватель, через который проходит 60000 м3/ч воздуха при температуре t1=15 °С и давлении Р=0.101 МПа. Температура воздуха после подогревателя равна 75 °С. Определить, какая часть теплоты топлива использована в подогревателе? К.П.Д. двигателя принять равным 0.33. Зависимость теплоемкости от температуры считать линейной. Ответ: 17.4%. 8.6. 2 м3 воздуха с начальной температурой t1=15 °С расширяются при постоянном давлении до 3 м3 вследствие сообщения газу 837 кДж теплоты. Определить конечную температуру, давление газа в процессе и работу расширения. Ответ: t2=159°С, Р=0.24 МПа, L=239 кДж. 8.7. Отходящие газы котельной установки проходят через воздухоподогреватель. Начальная температура газов tг1=300 °С, конечная tг2=160 °С; расход газов равен 1000 кг/ч. Начальная температура воздуха составляет tв1=15 °С, а расход его равен 910 кг/ч. Определить температуру нагретого воздуха tв2, если потери воздухоподогревателя составляют 4 %. Средние теплоемкости (cpm) для отходящих из котла газов и воздуха принять соответственно равными 1,0467 и 1,0048 кДж/кг К. Ответ: tв2=168,9 °С. 8.8. Определить, какая часть теплоты, подводимой к газу в изобарном процессе, расходуется на работу и какая - на изменение внутренней энергии. Решение: Аналитическое выражение первого закона термодинамики dq=du+dl может быть представлено в виде du/dq+dl/dq=1. Величина dl/dq=1-du/dq определяет ту долю от всей подводимой к газу теплоты, которая превращается в работу расширения. Так как для идеального газа в процессе Р=const du=cvdt и dq=cpdt, то dl/dq=1-cvdt/cpdt. Принимая к=1.4, получаем dl/dq=1-1/1.4=0.285. Следовательно, в изобарном процессе только 28.5% теплоты, подводимой к газу, превращается в работу. Вся остальная теплота, т.е. 71.5%, расходуется на увеличение внутренней энергии. Изотермический процесс Процесс сообщения или отнятия теплоты при постоянной температуре называется изотермическим. Уравнение процесса Зависимость между начальными и конечными параметрами в изотермическом процессе определяется формулами:
Работу 1 кг идеального газа находят их уравнений:
Если в процессе участвует М кг газа, то полученные из формул 9.3 – 9.6 значения нужно увеличить в М раз. Можно также для этого случая в формулах 9.5 и 9.6 заменить удельный объем
Так как в изотермическом процессе
Количество теплоты, сообщаемой газу или отнимаемой от него
или для М кг газа
Задачи 9.1. 1 кг воздуха при температуре t1=30°С и начальном давлении р1=0.1 МПа сжимается изотермически до конечного давления р2=1 МПа. Определить конечный объем, затрачиваемую работу и количество теплоты, отводимой от газа. Решение: Найдем начальный объем воздуха из уравнения состояния: v1=RT1/p1=287∙303/0.1∙106=0.87 м3/кг. Так как в изотермическом процессе p1v1=p2v2 то конечный объем v2=v1∙p1/p2=0.87∙1/10=0.087 м3/кг. Работа , затрачиваемая на сжатие 1 кг воздуха, получается из уравнения (9.8): L=RTlnp1/p2=2.303RTlnp1/p2=-2.303∙287∙303lg10=-200 кДж/кг. Количество теплоты, отводимой от газа, равно работе, затраченной на сжатие. Следовательно, q=-200кДж/кг. 9.2. Воздух в количестве 0.5 кг при р1=0.5 МПа и t1=30°С расширяется изотермически до пятикратного объема. Определить работу, совершаемую газом, конечное давление и количество теплоты, сообщаемой газу. Ответ: р2=0.1 МПа , L=Q=70 кДж. 9.3. Для осуществления изотермического сжатия 0.8 кг воздуха при р1=0.1 МПа и t=25°С затрачена работа в 100 кДж. Найти давление р2 сжатого воздуха и количество теплоты, которое необходимо при этом отвести от газа? Ответ: р2=0.322 МПа, Q=-90 кДж. 9.4. 8 м3 воздуха при р1=0.09 МПа и t1=20°С сжимаются при постоянной температуре до 0.81 МПа. Определить конечный объем, затраченную работу и количество теплоты, которое необходимо отвести от газа. Ответ: V2=0.889 м3, L=Q=-1581 кДж. 9.5. При изотермическом сжатии 0.3 м3 воздуха с начальными параметрами р1=1 МПа и t1=300°С отводится 500 кДж теплоты. Определить конечный объем V2 и конечное давление р2. Ответ: V2=0.057 м3, р2=5.26 МПа. 9.6. 10 кг воздуха при давлении р1=0.12 МПа и температуре t1=30°С сжимаются изотермически; при этом в результате сжатия объем увеличивается в 2.5 раза. Определить начальные и конечные параметры, количество теплоты, работу и изменение внутренней энергии. Ответ: V1=7.25 м3; V2=2.9 м3; p2=0.3 МПа; Q=L=-797 кДж; DU=0. Адиабатный процесс
где k=cp/cv - показатель адиабаты. Зависимости между начальными и конечными параметрами процесса: Между p и v: между T и v: между p и T:
Работу 1 кг газа находят по следующим формулам:
Для определения работы Тогда получим
Формула (9.6) для M кг газа примет следующий вид:
Уравнение первого закона для адиабатного процесса имеет вид:
следовательно, Изменение внутренней энергии идеального газа в адиабатном процессе может быть также выражено уравнением:
Задачи 10.1. 1 кг воздуха при начальной температуре t1=30 °С и давлении Р1=0.1 МПа сжимается адиабатно до конечного давления Р2=1 МПа. Определить конечный объем, конечную температуру и затрачиваемую работу. Решение: Из соотношения параметров в адиабатном процессе находим по уравнению T2/T1=(Р2/Р1)k-1/k, откуда T2=T1(Р2/Р1)k-1/k. Принимая к=1.4 , получаем Т2=303∙100.4/1.4=303∙100.286=303N; lgN=lg 100.286=0.286lg10=0.286; M=1.931; T2=303∙1.931=585 K; t2=312°С. Значение величины (Р2 /Р1)к-1/к для адиабатного сжатия при р2/p1=10 величина (Р2/Р1)к-1/к=1.931. Затраченная работа по уравнению (9.6) L=R∙ (T1-T2)/(k-1)=0.287∙(303-585)/0.4=-202 кДж/кг. Конечный объем определяется из уравнения состояния v2=RT2/Р2=287∙585/1∙106=0.168 м3/кг. 10.2. 1 кг воздуха при температуре t1=15°С и начальном давлении Р1=0.1 МПа адиабатно сжимается до 0.8 МПа. Найти работу , конечный объем и конечную температуру. Ответ: t2=248°С; v2=0.187 м3/кг; L=-167.2 кДж/кг. 10.3. Воздух при давлении Р1=0.45 МПа, расширяясь адиабатно до 0.12 МПа, охлаждается до t2=-45 °С. Определить начальную температуру и работу, совершенную 1 кг воздуха. Ответ: t1=61°С; L=75.3 кДж/кг. 10.4. 1 кг воздуха, занимающий объем v1=0.0887 м3/кг при Р1=1 МПа, расширяется до 10-кратного объема. Получить конечное давление и работу, совершенную воздухом, в изотермическом и адиабатном процессах. Ответ: 1). Т=const; Р2=0.1МПа ; L=204 кДж/кг; 2). dQ=0; p2=0.04 МПа; L=133.5 кДж/кг. 10.5. Воздух при температуре t1=25 °С адиабатно охлаждается до t2=-55 °С; давление при этом падает до 0.1 МПа. Определить начальное давление и работу расширения 1 кг воздуха. Ответ: Р1=0.3 МПа; L=57.4 кДж/кг. 10.6. Адиабатным сжатием повысили температуру воздуха в двигателе так, что она стала равной температуре воспламенения нефти, объем при этом уменьшился в 14 раз. Определить конечную температуру и конечное давление воздуха, если Р1=0.1 МПа и t1=100 °С. Решение: Конечную температуру определяем по формуле: T2=T1(v1/v2)k-1=373∙140.4=373∙2.86=1067 K. Конечное давление находим из уравнения (91) Р2=Р1(T2/T1)k/k-1=0.1(1067/373)1.4/0.4=0.1∙2.863.5=4 МПа. 10.7. Работа, затраченная на адиабатное сжатие 3 кг воздуха, составляет 471 кДж. Начальное состояние воздуха характеризуется параметрами: t1=15 °С; Р1=0.1 МПа. Определить конечную температуру и изменение внутренней энергии. Ответ: t2=234 °С ; DU=-471 кДж. 10.8. 1 м3 воздуха при давлении 0,095 МПа и начальной температуре 10°С сжимается по адиабате до 0,38 МПа. Определить температуру и объем воздуха в конце сжатия и работу, затраченную на сжатие. Ответ: t2=148 °С, V2=0.373 м3, L=-117 кДж. 10.9. 1 кг воздуха при температуре t1=17°С сжимается адиабатно до объема, составляющего 1/5 начального, а затем расширяется изотермически до первоначального объема. Определить работу, произведенную воздухом в результате обоих процессов. Ответ: L= 67 кДж/кг.
Политропный процесс Уравнение политропы в системе координат
где Характеристикой политропного процесса является величина
которая может быть определена из выражения
где Зависимости между начальными и конечными параметрами процесса: между между между Работу 1 кг газа находят по следующим формулам:
Если количество теплоты, участвующей в процессе, известно, то работа может быть также вычислена по формуле
Для определения работы M кг газа нужно в формулах (11.6) – (11.8)заменить удельный объем v полным объемом V газа. Тогда получим
Формулы (11.9) и (11.10) для M кг газа имеют следующий вид:
Теплоемкость политропного процесса можно найти из уравнения или, заменяя
Количество теплоты, сообщаемой газу или отнимаемой от него:
Величину
Изменение внутренней энергии газа в политропном процессе
Показатель политропного процесса
Задачи 11.1. 1 кг воздуха при р1=0.5 МПа и t1=111°С расширяется политропно до давления Р2=0.1 МПа. Определить конечное состояние воздуха, изменение внутренней энергии, количество подведенной теплоты и полученную работу, если показатель политропы n=1.2. Решение: Определяем начальный объем воздуха v1=RT1/Р1=(287∙384)/(0.5∙106)=0.22 м3/кг. Конечный объем воздуха находим из уравнения (11.3) v2=v1(Р1/Р2)1/n=0.22∙51/1.2=0.84 м3/кг. Конечную температуру проще всего получить из характеристического уравнения T2=Р2v2/R=0.1∙106∙0.84/287=293 K. Величину работы находим из уравнения (10.9) L=R(T1-T2)/(n-1)=287(384-293)/0.2=130 600 Дж/кг=130.6 кДж/кг. Изменение внутренней энергии Du=cv(T2-T1)=20.93(293-384)/28.96=-65.8 кДж/кг. Количество теплоты, сообщенной воздуху , по уравнению (11.17) q=cv(n - k)/(n - 1)·(t2-t1)=0.72(1.2-1.4)/(1.2-1) (20-111)=65.8 кДж/кг. Нетрудно видеть, что в этом процессе внешняя работа совершается за счет подведенной теплоты и уменьшения внутренней энергии. Исходя из этого можно проверить полученные результаты следующим образом: q=Du+L; L=q - Du=65.8-(-65.8)=131.6 кДж/кг. Этот же результат получен выше другим путем. 11.2. 1.5 кг воздуха сжимают политропно от р1=0.09 МПа и t1=18°С до р2=1 МПа, температура при этом повышается до t2=125°С. Определить показатель политропы, конечный объем, затраченную работу и количество отведенной теплоты. Решение: По формуле (n-1)/n=(lgT2/T1)/(lgp2/p1)=(lg398/291)/(lg100/9)=0.13, отсюда n=1/(1-0.13)=1.149. Конечный объем находим из характеристического уравнения V2=MRT2/p2=1.5∙287∙398/106=0.171 м3. Затраченная работа по уравнению (10.46) L=MR(t1-t2)/(n-1)=1.5∙287(18-125)/0.149=-309200 Дж=-309.2 кДж. Количество отведенной теплоты по уравнению Q=Mcv(n-k)/(n-1) (t2-t1)= =1.5∙20.93/28.96∙(1.149-1.4)/(1.149-1) (125-18)=-195.4 кДж. 11.3. Воздух в количестве 3 м3 расширяется политропно от р1=0.54 МПа и t1=45°С до р2=0.15 МПа. Объем, занимаемый при этом воздухом, становится равным 10 м3. Найти показатель политропы, конечную температуру, полученную работу и количество подведенной теплоты. Ответ: m=1.064, t2=21.4°С, L=1875 кДж, Q=1575 кДж. 11.4. В цилиндре двигателя с изобарным подводом теплоты сжимается воздух по политропе с показателем m=1.33. Определить температуру и давление воздуха в конце сжатия, если степень сжатия ( e=V1/V2) равна 14, t1=77°С и р1=0.1 МПа. Ответ: t2=564°С, р2=3.39 МПа. Знак плюс(+) показывает , что теплота в данном процессе подводится . Об этом можно судить также по величине показателя политропы. Изменение внутренней энергии DU= Q – L =672.4-1923=-1250.6 кДж. Знак минус (-) показывает, что внутренняя энергия убывает . В данном процессе работа совершается за счет подводимой извне теплоты, а также внутренней энергии газа. 11.5. В процессе политропного сжатия затрачивается работа , равная 195 кДж, причем в одном случае от газа отводится 250 кДж, а в другом - газу сообщается 42 кДж. Определить показатели обеих политроп. Ответ: 1). m=0.9, 2). m=1.49. 11.6. 1.5 м3 воздуха сжимаются от 0.1 МПа и 17°С до 0.7 МПа, конечная температура при этом равна 100°С. Какое количество теплоты требуется отвести, какую работу затратить и каков показатель политропы? Ответ: Q=-183 кДж, L=-290 кДж, m=1.147. 11.7. 0.01 м3 воздуха при давлении р1=1 МПа и температуре t1=25°С расширяется в цилиндре с подвижным поршнем до 0.1 МПа. Найти конечный объем, конечную температуру, работу, произведенную газом, и подведенную теплоту, если расширение в цилиндре происходит: а)изотермически, б)адиабатно и в)политропно с показателями m =1.3. Решение: а). Изотермическое расширение. Конечный объем определяют по формуле (11.11) V2=V1p1/p2=0.01∙1/0.1=0.1 м3. Так как в изотермическом процессе t=const, то конечная температура t2=t1=25°С. Работа газа по уравнению (10.17) L=p1V1lnp1/p2=1∙106∙0.01∙2.303lg10=23 000 Дж. Количество подведенной теплоты по формуле (11.19) Q=L=23 кДж. б). Адиабатное расширение. Конечный объем определяется по уравнению (11.20) V2=V1(p1/p2)1/k=0.01∙101/1.4. Пользуясь табл. XIX, получаем 101/1.4=5.188. Следовательно V2=0.01∙5.188=0.05188 м3. Конечная температура воздуха на основании уравнения (11.22) T2=T1(p2/p1)k-1/k=298(0.1/1)1.4-1/1.4=154.3 K; t2=-118.7°С. Работа газа по уравнению (10.29) L=p1V1/(k-1) (1-(p2/p1)k-1/k)=1∙106∙0.01/0.4∙(1-1/1.931)= =25000∙0.48=12 000Дж=12 кДж. в). Политропное расширение. Конечный объем найдем из уравнения (11.35) V2=V1(p1/p2)1/m=0.01∙101/1.3=0.01∙5.885=0.05885 м3. Конечная температура по уравнению (10.37) T2=T1(p1/p2)m-1/m=298(0.1/1)0.3/1.3=175.2 K; t2=-97.8 °С. Работа газа по уравнению (10.45) L=p1V1/(m-1) (1-(p2/p1)m-1/m)= =1∙106∙0.01/0.3∙(1-(0.1/1)0.3/1.3)=13700 Дж=13.7 кДж. Подведенная теплота по уравнению (10.50) Q=L(k-m)/(k-1)=13.7∙0.1/0.4=3.425 кДж. 11.8.В процессе политропного расширения воздуху сообщается 83.7 кДж тепла. Найти изменение внутренней энергии воздуха и произведенную работу, если объем воздуха увеличился в 10 раз, а давление его уменьшилось в 8 раз. Ответ: DU=16.7 кДж; L=6702 кДж. 11.10. Воздух расширяется по политропе, совершая при этом работу, равную 270 кДж, причем в одном случае ему сообщается 420 кДж теплоты, а в другом - от воздуха отводится 92 кДж теплоты. Определить в обоих случаях показатели политропы. Ответ: 1). m=0.78; 2). m=1.88. 11.11. 2 м3 воздуха при давлении р1=0.09 МПа и температуре t1=40°С сжимаются до давления р2=1.1 МПа и объема V2=0.5 м3. Определить показатель политропы, работу сжатия и количество отведенной теплоты.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|
 ,
, (7.1)
(7.1) (7.2)
(7.2)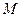 кг или
кг или 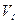 м3 газа, то количество теплоты или изменение внутренней энергии газа
м3 газа, то количество теплоты или изменение внутренней энергии газа (7.3)
(7.3) (8.1)
(8.1) (8.2)
(8.2) . (8.3)
. (8.3) (8.4)
(8.4) . (8.5)
. (8.5) участвует М кг или Vн м3 газа, то количество теплоты
участвует М кг или Vн м3 газа, то количество теплоты (8.6)
(8.6) (9.1 )
(9.1 ) ( 9.2)
( 9.2)
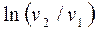 ; (9.3)
; (9.3) ; (9.4)
; (9.4)
 ; (9.5)
; (9.5)
 . (9.6)
. (9.6) полным объемом
полным объемом  . Тогда получим
. Тогда получим
 ; (9.7)
; (9.7)
 . (9.8)
. (9.8) , то для идеального газа изменение внутренней энергии равно
, то для идеального газа изменение внутренней энергии равно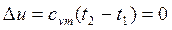 .
. (9.9)
(9.9) (9.10)
(9.10) ,
, , (10.1)
, (10.1) , (10.2)
, (10.2) . (10.3)
. (10.3) ; (10.4)
; (10.4) ; (10.5)
; (10.5) ; (10.6)
; (10.6) . (10.7)
. (10.7) (10.8)
(10.8) ; (10.9)
; (10.9) . (10.10)
. (10.10) ;
; , (10.12)
, (10.12) или
или  , т.е. изменение внутренней энергии газа и работа адиабатного процесса равны по величине и противоположны по знаку.
, т.е. изменение внутренней энергии газа и работа адиабатного процесса равны по величине и противоположны по знаку. . (10.13)
. (10.13) при постоянной теплоемкости
при постоянной теплоемкости ,
, - показатель политропы.
- показатель политропы. , (11.1)
, (11.1) , (11.2)
, (11.2) .
. и
и 
 , (11.3)
, (11.3) и
и 
 , (11.4)
, (11.4) и
и 
 . (11.5)
. (11.5) ; (11.6)
; (11.6) ; (11.7)
; (11.7) ; (11.8)
; (11.8) . (11.9)
. (11.9) . (11.10)
. (11.10) ; (11.11)
; (11.11) ; (11.12)
; (11.12) ; (11.13)
; (11.13) ; (11.14)
; (11.14) . (11.15)
. (11.15) ,
, его значением из уравнения (11.2), получим
его значением из уравнения (11.2), получим .
. (11.16)
(11.16) (11.17)
(11.17) можно также определить из формулы (11.15), если известна работа политропного процесса:
можно также определить из формулы (11.15), если известна работа политропного процесса: . (11.18)
. (11.18)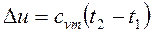 . (11.19)
. (11.19) определяется из уравнения
определяется из уравнения . (11.20)
. (11.20) Ответ: m=1.23; L=-652 кДж; Q=-272 кДж.
Ответ: m=1.23; L=-652 кДж; Q=-272 кДж.