
|
|
Дисперсные системы, их свойства, органическая устойчивость дисперсных системБроуновское движение. Диффузия. Седиментация и седиментационное равновесие. Методы седиментационного анализа. Осмотическое давление. Рассеяние света (опалесценция) и флуктуации. Эффект Фарадея-Тиндаля. Абсорбция (поглощение) света и окраска ультрамикрогетерогенных систем (коллоидных растворов). Оптические методы исследования дисперсных систем. Нефелометрия, световая, ультра- и электронная микроскопии. Молекулярные взаимодействия и особые свойства поверхностей раздела фаз. Классификация, характеристика адгезии, когезии, смачивания, растекания. Практическое применение поверхностных явлений Поверхностные явления. Поверхностная энергия. Поверхностное натяжение. Характер влияния температуры, концентрации растворенных веществ и их природы на величину поверхностного натяжения. Метод определения поверхностного натяжения жидкостей и твердых тел. Классификация поверхностных явлений по способу уменьшения поверхностной энергии. Характеристика поверхностных явлений, сопровождающихся изменением формы поверхности раздела фаз. Смачивание иммерсионное и контактное. Краевой угол смачивания. Растекание. Поверхностные пленки, их свойства. Когезия и адгезия. Вязкость. Капиллярные явления (капиллярное поднятие жидкости, капиллярная конденсация).
Адсорбционные слои, их влияние на свойства дисперсных систем. Сорбционные процессы. Адсорбция. Теории Гиббса, Ленгмюра, БЭТ и другие. Капиллярная конденсация Сорбция и сорбционные процессы. Адсорбция, общее представление и закономерности. Классификация адсорбции по агрегатному состоянию смежных фаз. Адсорбция на поверхности раздела жидкость – газ. Уравнение Гиббса. Поверхностно-активные вещества. Ориентация на поверхности раздела фаз. Адсорбция на поверхности раздела твердое тело – газ и твердое тело – жидкость. Адсорбенты: активированный уголь, гели, цеолиты. Динамический характер адсорбционного равновесия. Природа адсорбционных сил. Хемосорбция. Изотермы адсорбции. Уравнение Фрейндлиха-Бедекера. Уравнение Лэнгмюра. Переход от уравнения Гиббса к уравнению Лэнгмюра. Теория полимолекулярной адсорбции БЭТ. Потенциальная теория Поляни. Теория объемного заполнения микропор Дубинина. Адсорбция электролитов. Образование двойного электрического слоя. Ионообменная адсорбция. Иониты и их применение. Адсорбционная хроматография. Электрические свойства коллоидных растворов Строение частиц лиофобных золей. Правило Фаянса и Содди достройки кристаллической решётки. Строение двойного электрического слоя. Теории Гельмгольца, Гуи-Чемпена, Штерна. Поверхностный и электрокинетический потенциалы. Электрокинетический катализ. Электрокинетические явления прямые (электрофорез) и обратные (эффекты Дорна и Квинке). Диспергирование, физическая и химическая конденсация, пептизация. Очистка коллоидных растворов от избытка электролитов и низкомолекулярных соединений ультрафильтрацией и методом диализа. Электродиализ. Компенсационный диализ. Применение диализа.
Устойчивость коллоидных растворов. Коагуляция Кинетическая и агрегативная устойчивость. Факторы устойчивости. Коагуляция под действием электролитов. Порог коагуляции. Критический потенциал. Правило значности. Коагуляция смесью электролитов. Явления синергизма и антагонизма. Взаимная коагуляция коллоидных растворов. Явление привыкания. Кинетика коагуляции. Теория коагуляции.
Растворы высокомолекулярных соединений (ВМС). Коллоидные ПАВ Общая характеристика ВМС. Термодинамическая устойчивость ВМС. Растворы высокомолекулярных электролитов. Белки как полиэлектролиты. Влияние pH на свойства растворов белков. Изоэлектрическое состояние. Денатурация, высаливание, коацервация. Лиотропные ряды. Защита гидрофобных золей ВМС. Применение явления защиты. Вязкость коллоидных растворов (нормальная и аномальная). Приведенная и характеристическая вязкость. Вискозиметрический метод определения молекулярной массы полимеров. Микрогетерогенные системы: гели, суспензии, эмульсии, аэрозоли Классификация гелей. Теория строения. Методы получения. Желатинирование. Факторы, влияющие на набухание. Явления набухания в природе. Тиксотропия, синерезис. Диффузия в студнях, реакции в студнях. Классификация эмульсий. Устойчивость разбавленных и концентрированных эмульсий. Жидкие и твердые эмульгаторы. Механизм стабилизации эмульгаторами. Метод получения и разрушения эмульсий. Обращение эмульсий. Практическое значение эмульсий и эмульгирования. Жидкие пены. Методы получения и разрушения пен. Устойчивость пен. Пенообразователи. Теория пенообразования. Практическое значение пен. Моющие вещества и теория моющего действия. Пенная флотация. Твердые пены (пенобетон, пеностекло, пенопласт). Общая характеристика. Туманы. Дымы и пыль. Методы получения и разрушения аэрозолей. Проблемы защиты атмосферы от загрязнения аэрозолями. Коллоидно-дисперсные системы почвы. Темы практических и/или семинарских занятий Учебным планом не предусмотрены.
Лабораторные работы Лабораторные работы проводятся в специализированной лаборатории «Физической химии», оснащённой необходимым оборудованием: измерительным оборудованием, электрооборудованием, реактивами и лабораторной посудой
Вопросы к коллоквиумам в рамках лабораторных работ. Тема I. Общая характеристика дисперсных систем и их молекулярно-кинетические свойства 1. Что изучает коллоидная химия и каковы признаки ее объектов? 2. По каким признакам классифицируют объекты коллоидной химии?Приведите примеры дисперсных систем? 3. Каковы основные методы получения и очистки дисперсных систем? 4. Какими параметрами характеризуют степень раздробленности и какова связь между ними? 5. Как можно определить размеры дисперсных частиц или концентрацию их в лиозолях по осмотическому давлению? 6. Что называется коэффициентом диффузии и на основании каких измерений он может быть определен? 7. Что такое седиментацонно-диффузионное равновесие? Как определяют размеры частиц в условиях этого равновесия?
Тема 2. Оптические свойства дисперсных систем 1. Какие оптические явления наблюдаются при падении луча на дисперсную систему? Какие методы исследования дисперсных систем основаны на этих явлениях? 2. Какие оптические методы используются для определения размеров частиц дисперсных систем? 3. Чем обусловлено светорассеяние в дисперсных системах и истинных растворах? Какими параметрами количественно характеризуют рассеяние света в системе? 4. Какие золи называют "белыми"? Какова связь между оптической плотностью и мутностью белых золей? Для каких дисперсных систем применимо уравнение Рэлея? 5. Как влияют размеры частиц на зависимость оптической плотности "белых" золей от длины волны падающего света? 6. Чем различаются методы нефелометрии и турбидиметрии? Какие уравнения используются для определения характеристик рассеяния света? 7. Для каких дисперсных систем применимо уравнение Дебая? Какие параметры дисперсных систем определяют по методу Дебая?
Тема 3. Поверхностные явления и адсорбция 1. Что такое поверхностное натяжение и в каких единицах оно измеряется? Как зависит поверхностное натяжение от природы вещества, образующего поверхность (межмолекулярного взаимодействия)? 2. Какие методы используются для определения поверхностного натяжения? Поясните суть этих методов. 3. Что называется адсорбцией и как количественно ее характеризуют? Напишите фундаментальное адсорбционное уравнение Гиббса и дайте определение избыточной адсорбции. 4. Что такое поверхностная активность? Какие вещества называются поверхностно-активными? 5. Что называют адгезией и смачиванием? Какие параметры используют для их количественной характеристики? 6. Как влияет природа твердого тела и жидкости (межмолекулярное взаимодействие в них) на смачивание и адгезию? 7. Дайте характеристику и приведите примеры гидрофильных и гидрофобных поверхностей. Как можно повлиять на смачивание поверхности? 8. Чем обусловлено улучшение смачивания водой гидрофобных поверхностей при введении в нее ПАВ? 9. Как рассчитать толщину адсорбционного слоя и «посадочную» площадку молекул ПАВ, зная зависимость поверхностного натяжения от состава раствора?
Тема 4. Электрокинетические свойства дисперсных систем 1. Каковы возможные причины возникновения двойного электрического слоя на межфазной поверхности? Приведите примеры механизмов образования двойного электрического слоя в различных дисперсных системах. 2. Дайте характеристику строения двойного электрического слоя на поверхности раздела фаз. Как изменяется потенциал с расстоянием от поверхности? 3. Расскажите об основных положениях теории строения двойного электрического слоя. Что понимают под толщиной диффузной части ДЭС? Чем определяется толщина плотной и диффузной частей ДЭС? 4. Каким закономерностям подчиняется адсорбция ионов? Изобразите строение коллоидных частиц, несущих: а) положительный заряд, б) отрицательный заряд. Укажите на схемах составные части мицелл. 5. Перечислите электрокинетические явления и объясните, чем они обусловлены. 6. Что такое нулевые точки заряда и изоточки, какими методами они исследуются в различных системах, как изменяются в зависимости от состава среды? 8. Каковы основные эффекты взаимодействия коллоидных систем с нейтральными солями? В чем выражаются специфические явления при этом взаимодействии? Как изменяется структура двойного слоя в результате этого взаимодействия?
Тема 5. Устойчивость и коагуляция лиофобных коллоидов I. Чем определяется агрегативная устойчивость лиофобных коллоидов, чем она отличается от кинетической устойчивости? 2. В чем заключается правило Шульце-Гарди? В каком соотношении находятся пороги коагуляции для различных ионов? 3. Каким образом происходит сокращения толщины двойного слоя при коагуляции коллоидов электролитами и почему оно приводит к коагуляции? 4. Какой процесс называют коагуляцией? Чем завершается процесс коагуляции? Какими способами можно вызвать коагуляцию лиофобной коллоидной системы? 5. Что такое потенциальные кривые взаимодействия коллоидных частиц и каков их характер? Каким образом на их основе объясняются явления коагуляции и тиксотропии? 6. Действием каких факторов обеспечивается агрегативная устойчивость лиофобных дисперсных систем? Какие вещества используют в качестве стабилизаторов этих систем? 7. В чем заключается пептизация и какими методами она осуществляется? 8. Чем определяется значение сольватных слоев для устойчивости коллоидов? 9. Какое значение для устойчивости имеют адсорбционные слои поверхностно-активных веществ и чем оно определяется? 10. В чем заключается защитное действие и сенсибилизация?
Тема. 6. Образование и свойства лиофильных коллоидов 1. По какому признаку дисперсные системы делят на лиофобные и лиофильные? Чем объяснить самопроизвольное возрастание межфазной поверхности при образовании лиофильных дисперсных систем? 2. Какой параметр используется в качестве критерия лиофильности дисперсной системы? 3. Какие дисперсные системы относят к лиофильным? Приведите примеры таких систем. Как происходит формирование частиц дисперсной фазы в лиофильных системах? 4. Чем отличаются коллоидные ПАВ от истинно растворимых? Что называют критической концентрацией мицеллообразования? 5. Какие существуют методы определения ККМ? Почему при концентрациях, превышающих ККМ, поверхностное натяжение растворов ПАВ практически не изменяется? 6. Какие факторы влияют на ККМ? Как и почему влияет длина углеводородного радикала на ККМ в разных по полярности растворителях? 7. Каким образом ориентируются молекулы ПАВ в мицеллах, образующихся в полярной и неполярной средах? От чего зависит форма мицелл в растворах коллоидных ПАВ? 8. Как влияет на ККМ природа полярной группы молекул ПАВ? Каково влияние добавок индифферентного электролита на ККМ ионогенных и неионогенных ПАВ? 9. Какое явление называют солюбилизацией? Чем обусловлено это явление? Каково практическое значение этого явления? 10. Расскажите о практическом применении ПАВ. На чем основано использование ПАВ в качестве стабилизаторов дисперсных систем? В чем заключается механизм моющего действия растворов ПАВ? 11. Каковы особенности растворения полимеров? Какой процесс называется набуханием? В каких случаях происходит ограниченное и неограниченное набухание полимера? Укажите характеристики набухания полимеров в низкомолекулярных

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|
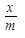 – lg Сi и по нему определить а и n в уравнении Фрейндлиха-Бедекера.
– lg Сi и по нему определить а и n в уравнении Фрейндлиха-Бедекера.