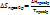|
|
Изменение энтропии при изотермическом расширении или сжатии.Для расчета энтропии в этом случае нужно найти ур-е состояния системы. Расчет основан на исп-нии соотношения Максвелла:
В частности, при изотерм. расширении идеального газа (p=nRT/V)
Этот же рез-тат можно получить, если исп-ть выражение для изотерм-ки обратимого расширения ид. газа: Qобр=nRT·ln(V2/V1) Применение третьего закона термодинамики для расчета равновесий. Существует два метода: 1 метод основывается на определении абсолютного значения 2 метод основывается на химически постоянных (Нернстон) В первом методе Кр химич. реакции и выход вычисления из уравнений:
Решение второй части – выходы реакции треб. знание абсол. величин S. Например, в общем виде для реакции А+В=2Д
Знание третьего з-на для расчетов равновесий состоит в том, что он дает возможность найти величины энтропии, участвующих в реакции. Интегрирование обычно проводят графическим методом
Изменение свободной энергии при изотермическом расширении и сжатии Свободная энергия [F]— термодинамический потенциал, убыль которого в квазистатическом изотермическом процессе равна работе, совершённой системой над внешними телами. В механике энергия тела равна сумме потенциальной и кинетической энергий. Оба этих вида энергий макроскопических тел могут быть полностью преобразованы в механическую работу. Внутренняя энергия молекулярной системы, в интересующем нас случае, не может быть целиком превращена в работу. Посмотрим, чем отличаются свободная энергия и внутренняя . При изотермическом расширении идеального газа от объема до объема работа одного моля В изотермическом процессе сжатый газ совершает работу за счет подводимого тепла, но мы говорим о свободной энергии газа, т.к. работу совершает газ. В общем случае, когда процесс протекает необратимо, совершаемая работа меньше чем в обратимом процессе, т.е. меньше чем изменение свободной энергии. TdS>δQ, δA< -dF Возможны так же случаи, когда изменение свободной энергии не сопровождается совершением работы, например, расширение газа в пустоту. Работ не совершается, внутренняя энергия не изменяется, а способность совершать работу падает. Это так, потому что процесс расширения газа в пустоту необратим полностью, хотя и изотермический. Свободная энергия , так же как и внутренняя энергия является функцией состояния системы. А это вытекает из того, что при обратимом изотермическом процессе, при переходе из состояния 1 в состояние 2 и обратно в 1, работа ΔA=0 следовательно, в таком переходе работа не зависит от пути, а только от начального и конечного состояния системы. Рассмотрим I начало для изотермического процесса δA=-(dU-dTS)=-d(TS-U)=-dF ТД системы будет условие минимума свободной энергии. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|


 ;
;  - стандартное состояние т.о. сводится к нахождению теплового эффекта. Для решения первой части (∆Н) требуется знание ∆СР(Т) реакции и величины ΔH0 при одной температуре, что позволяет при помощи уравнения Кирхгофа вычислить постоянную
- стандартное состояние т.о. сводится к нахождению теплового эффекта. Для решения первой части (∆Н) требуется знание ∆СР(Т) реакции и величины ΔH0 при одной температуре, что позволяет при помощи уравнения Кирхгофа вычислить постоянную  и тем самым
и тем самым  , при любой температуре:
, при любой температуре: