
|
|
Расчёт продуктов электролизаВведение
Насчитывается более 250 минералов алюминия, которые преимущественно сосредоточены вблизи поверхности земли, и более 40 % из них относится к алюмосиликатам. Алюминий уже давно является промышленным металлом, так как он обладает рядом свойств, которые выгодно отличают его от других металлов. Для него характерны: небольшая плотность; хорошая пластичность и достаточная механическая прочность; высокая тепло- и электропроводность, коррозионная устойчивость. Важнейшие потребители алюминия и его сплавов – авиационная и автомобильная промышленность, железнодорожный и водный транспорт, машиностроение, электротехническая, химическая, металлургическая и пищевая промышленности, промышленное и гражданское строительство. В металлургической промышленности алюминий применяют в качестве восстановителя при получении ряда металлов (хрома, кальция и пр.) алюмотермическими способами, для сварки стальных деталей. Конструкции из алюминия требуют более низких затрат в течение срока службы и практически не требуют ремонта. Обладая хорошей гибкостью, алюминиевые конструкции эффективно несут нагрузки и значительно снижают затраты на сооружение фундаментов и опор. Алюминий способен образовывать сплавы со многими металлами. Алюминиевые сплавы делятся на две группы: литейные сплавы, которые применяются для фасонного литья, и деформируемые сплавы, идущие на производство проката и штампованных изделий. Из литейных сплавов наиболее распространены сплавы алюминия с кремнием, называемые силуминами.
Расчётная часть Для получения алюминия - сырца в электролизёр загружают глинозём, анодную массу и фторсоли. В процессе электролиза образуются в основном окислы углерода. В результате испарения и пылеуноса отходящими газами из процесса постоянно выбывают некоторые количества фтористых соединений и глинозёма. При применении самообжигающихся анодов в процессе электролиза часть анодной массы выбывает в виде летучих соединений при коксовании анода. Кроме того, анодная масса расходуется в виде пены снимаемой с поверхности электролита. Увеличенный расход анодной массы и фтористых солей на электролизёрах с верхним токоподводом объясняется низким качеством анодной массы и недостатками обслуживания электролизёра. Материальный баланс
В процессе электролиза криолитоглинозёмного расплава расходуется глинозём, фтористые соли и угольный анод. При этом образуется расплавленный алюминий и газообразные оксиды углерода. Расчет веду на основании заданных параметров: - сила тока I=175 кА - анодная плотность тока dа = 0,71 А/см2 - выход по току h =88 % Расход сырья N кг на получение 1 кг алюминия - глинозем, NГ = 1,926кг - фтористый алюминий, NФа = 0,029кг - фтористый кальций, NCа = 0,0014кг - анодная масса, NМ = 0,546 кг Проектируемый цех состоит из 3 серий.. Производительность электролизера
Производительность электролизера РА1, кг рассчитывается по закону Фарадея:
РА1 = j * I * τ * h, (1)
где : j - электрохимический эквивалент алюминия, 0,335 кг/(кА*час); I - сила тока, кА; τ - время, час; - выход по току, доли единицы. P А1 = 0,335 * 175 * 0,88 = 51,59 кг Расчёт прихода сырья в электролизёр
Приход материалов в электролизёр рассчитывают исходя из норм расхода на 1кг алюминия и производительности электролизёра в час PAl. Затраты по сырью составят - глинозема RГ, кг RГ = PAl * NГ (2) RГ = 51,59 * 1,926 = 99,36 кг - фтористых солей (А1F3,СаF2 ) RФ, кг RФ =PAl * (NФа+ NCa) (3) RФ = 51,59 * ( 0,029 + 0,0014) = 1,568 кг - анодной массы Rм, кг Rм = PAl * Nоа (4) Rм = 51,59 * 0,546 = 28,168 кг Расчёт продуктов электролиза
Количество анодных газов рассчитывают исходя из их состава и реакций, протекающих в электролизёре. Для расчета принимаю состав анодных газов, % (масс.): СO2 - 60; СО - 40. При получении 46,4 алюминия выделится кислорода m0, кг:
где 48 и 54 – молярная масса соответственно кислорода и алюминия в глиноземе.
Из этого количества в двуокись углерода свяжется кислорода m0co2, кг:
в окись углерода свяжется кислорода m0co, кг:
где 60 и 40 – процентное содержание оксида углерода (CO2) и окиси углерода (СО) соответственно.
Отсюда можно рассчитать количество углерода связанного в двуокись mcco2, кг:
Количество углерода связанного в оксид углерода, mcco, кг:
Таким образом, в час выделяется оксидов Pco2 и Pco, кг: Pco2 = m0co2 + mcco2 Pco2 = 34,392 + 12,897 = 47,289 кг Pco = m0co + mcco (11) Pco = 11,464 + 8,59 = 20,054 Всего образуется анодных газов Ргаз, кг: Ргаз = Pco2 + Pco (12) Ргаз = 47,289 + 20,054 = 67,343 кг Расчёт потерь сырья
Теоретический расход глинозема составляет 1,89 кг на 1 кг алюминия. Перерасход глинозема объясняется наличием в его составе примесей и механическими потерями. Тогда потери глинозема G, кг составят: G = PAl * (Nг - 1,89) (13) G = 51,59* (1,926– 1,89 ) = 1,857 Потери углерода Rуг, кг находят по разности прихода анодной массы Rм и расхода углерода, связанного в окислы: Rуг = Rм - (mcco2 + mcco) (14) Rуг =28,168– (12,897+8,59) =6,681 кг Приход фторсолей в электролизёр принимаем равным их расходу. Таблица 1-Материальный баланс электролизера на силу тока 175кА.
*С учетом образования анодных газов и механических потерь
Конструктивный расчет В задачу конструктивного расчета входит определение основных размеров электролизера. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|
 (5)
(5) кг
кг (6)
(6) кг
кг (7)
(7) кг
кг (8)
(8) кг
кг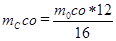 (9)
(9) кг
кг (10)
(10)