
|
|
Порядок выполнения работыОзнакомьтесь с методическими указаниями к лабораторной работе Ознакомьтесь с теорией в конспекте и учебнике. Введение. Порядок работы с программой В данной лабораторной работе используются компьютерные модели, разработанные фирмой «Физикон»: «Виртуальный практикум для ВУЗов» или «Открытая Физика» версия 2.5 часть 1. Для начала работы необходимо запустить программу, для чего дважды щелкнуть левой кнопкой мыши, когда ее маркер расположен над эмблемой сборника компьютерных моделей. После этого появится начальная картинка, имеющая вид
Рисунок 3 Начальная картинка «Виртуального практикума по физике для ВУЗов» Для программы «Открытая Физика» Версия 2.5 часть 1появится начальная картинка, имеющая вид
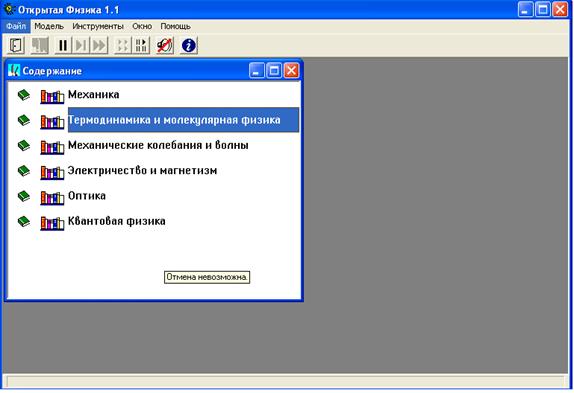
Рисунок 4 Начальная картинка «Открытая Физика» Версия 2.5 часть 1 После открытия начальной картинки для программы «Виртуальный практикум по физике» необходимо дважды щелкнуть левой кнопкой мыши, установив ее маркер над названием раздела, в котором расположена данная модель. Для раздела «Термодинамика и молекулярная физика» вы увидите следующую картинку
Рисунок 5 Начальная картинка для раздела «Термодинамика и молекулярная физика»
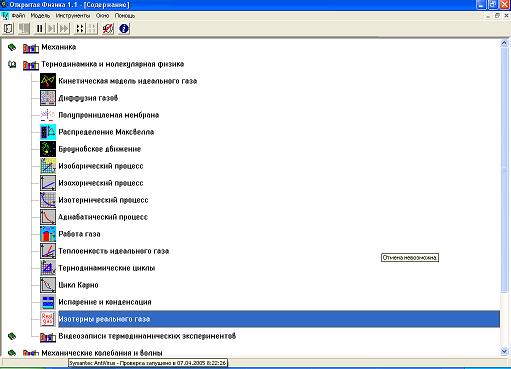
Для программы «Открытая Физика» Версия 2.5 часть 1 войдите раздел «Модели». После этого необходимо дважды щелкнуть левой кнопкой мыши, установив ее маркер над названием раздела, в котором расположена данная модель. 5.3 Методика и порядок измерений Выберите «Термодинамика и молекулярная физика», «Изотермы реального газа». Нажмите кнопку с изображением страницы во внутреннем окне.
Рисунок 6 Динамическая модель для лабораторной работы «Исследование состояния газа Ван-дер-Ваальса»
Прочитайте теорию и запишите необходимое в свой конспект лабораторной работы. Закройте окно теории, нажав кнопку с крестом в правом верхнем углу внутреннего окна. Внимательно рассмотрите рисунок и зарисуйте необходимое в свой конспект лабораторной работы. Внимательно рассмотрите картинку на рисунке, найдите рисунок элемента, в котором реализуется адиабатический процесс, обратите внимание на его теплоизоляцию. Найдите математическую формулировку условия теплоизоляции. Ознакомьтесь с графиками в правой части изображения. Зарисуйте необходимое в свой конспект лабораторной работы. Получите у преподавателя допуск для выполнения измерений. Измерения ЭКСПЕРИМЕНТ 1. ОПРЕДЕЛЕНИЕ КРИТИЧЕСКИХ ПАРАМЕТРОВ 1 Щелкните левой кнопкой мыши, когда ее маркер на кнопке «Выбор». 2 Подведите маркер мыши к кнопке у верхней границы столбика на регуляторе температуры и нажмите левую кнопку мыши. Удерживая кнопку в нажатом состоянии, перемещайте границу столбика до тех пор, пока на правом экране не появится критическая изотерма с точкой перегиба и без экстремумов. 3 Запишите в свой конспект значения критических параметров ТКР, VКР, pКР .
ЭКСПЕРИМЕНТ 2. ИССЛЕДОВАНИЕ ИЗОТЕРМ ГАЗА ВдВ. 1 Установите значение температуры, указанное первым в таблице начальных значений для вашей бригады. Нажмите мышью кнопку «СТАРТ» на экране и наблюдайте перемещение поршня на левой картинке модели и перемещение точки по красной кривой теоретической адиабаты. Попробуйте останавливать процесс нажатием кнопки «Стоп» на экране. Последующий запуск процесса осуществляется нажатием кнопки «Старт». 2 После остановки процесса запустите его снова, нажав кнопку «Старт», и останавливайте, нажимая кнопку «Стоп», когда крестик на теоретической изотерме (красная кривая) будет находиться вблизи следующих значений объема: 0.1, 0.12, 0.14, 0.16, 0.18 и 0.2 дм3 (6 значений), записывая при остановке значения в таблицу 2. 3 Установив новое значение температуры Т из таблицы 1, задавая Vнач = 0.1 дм3, повторите измерения, записывая результаты в таблицы 3,4,5. ТАБЛИЦА 1. Примерные значения температуры(не перерисовывать)
ТАБЛИЦЫ 2,3,4,5 Результаты измерений при Т = ____ К
5.5 Обработка результатов и оформление отчета: По измеренным значениям критических параметров вычислите константу А = Постройте на одном рисунке графики экспериментальных зависимостей давления от обратного объема для измеренных точек всех изотермических процессов (указав на них температуры). Для каждой изотермы определите значение количества вещества, используя
Вычислите среднее значение n и величину константы А’ по формуле А’ = 0,375n . Запишите ответ для А’ и проанализируйте ответы и графики. В выводах по ответу сравните А’, полученное по изотермам, с А, полученным через критические параметры. 6 Контрольные вопросы
1. Что такое физический газ? 2. Перечислите все известные агрегатные состояния вещества. 3. Что такое идеальный газ? 4. При каких условиях физический газ можно описывать моделью идеальный газ? 5. Что такое уравнение состояния? 6. Как выглядит уравнение состояния идеального газа? Каково его второе название? 7. Что такое газ Ван-дер-Ваальса? 8. Как выглядит уравнение состояния газа Ван-дер-Ваальса? Каково его второе название? 9. Что такое константы Ван-дер-Ваальса? 10. Что определяет первая константа Ван-дер-Ваальса? 11. Что определяет вторая константа Ван-дер-Ваальса? 12. Что такое изотерма? 13. Что такое критическая изотерма? 14. Каковы особенности поведения газа при температуре, выше критической? 15. Каковы особенности поведения газа при температуре, ниже критической? 16. На каких участках изотермы ВдВ примерно совпадают с изотермами реального газа? Содержание отчёта 7.1 Наименование работы. 7.2 Цель работы. 7.3 Описание используемого оборудования. 7.4 Краткое описание хода работы. Уравнения газа Ван-дер-Ваальса и уравнения для критических параметров. 7.5 Таблицы полученных данных. 7.6 Расчёт константы по измеренным значениям критических параметров. 7.7. Графики давления от обратного объема для измеренных точек всех изотермических процессов (указав на них температуры). 7.8. Расчёт количества вещества для каждой изотермы, среднего значения n и величины константы А’ по формуле А’ = 0,375n 7.9 Выводы. Список использованной литературы
1. Трофимова Т.И. Курс физики. М.: Высшая школа, 2001. Гл.10, §§ 60-62. 2. Детлаф А.А., Яворский Б.М. Курс физики. М.: Высшая школа, 2000. Гл. 12, §§ 12.1, 12.2. 3. Лукьянов А.Б. Физическая и коллоидная химия: Учебник для техникумов. – 2-е изд., перераб. И доп. – М.: Химия, 1988. – 288 с.: ил.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|

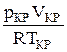 . (5)
. (5)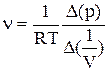 . (6)
. (6)