|
|
Механизм трансляционного контроля ооцитных мРНКВ настоящее время предложено по крайней мере пять гипотез относительно регуляции трансляции ооцитных мРНК. Три из них касаются доступности молекул мРНК, тогда как две другие – эффективности трансляции мРНК. Эти гипотезы могут рассматриваться как конкурирующие друг с другом, однако вполне вероятно, что у большинства видов регуляция трансляции ооцитных мРНК осуществляется с помощью нескольких механизмов. МАСКИРОВАННЫЕ мРНК. Согласно этой гипотезе, ооцитные мРНК физически замаскированы белками, поэтому мРНК не могут присоединиться к рибосоме. мРНК никогда не обнаруживается свободной от белков. Однако с мРНК могут быть ассоциированы белки различного типа. В 1966 г. Спирин предположил, что мРНК ооцита запасена в информосомах, рибонуклеопротеидных комплексах, где мРНК закрыта белками (Spirin, 1966). Эти замаскированные мРНК не способны связываться с рибосомами и поэтому не транслируются. При оплодотворении белки, экранирующие мРНК, отделяются (возможно, из-за изменений ионных условий, происходящих в ходе оплодотворения) и мРНК высвобождается, чтобы инициировать трансляцию. Вскоре эта гипотеза была подтверждена. В 1968 г. в ооцитах морского ежа были обнаружены рибонуклеопротеидные (РНП) частицы, которые седиментировали медленнее, чем рибосомы (Infante, Nemer, 1968), а несколько позже было обнаружено, что эти частицы содержат разнообразные мРНК (Gross et al., 1973). Серия экспериментов в лаборатории Рэффа показала, что ооцитная мРНК действительно запасается в такой форме, которая не способна к трансляции и чувствительна к ионным изменениям, происходящим при оплодотворении. Нерибосомные РНП-частицы выделили из зрелых ооцитов морского ежа и выяснили, что они содержат РНК с поли(А)-хвостами (Jenkins et al., 1978). Таким образом, эти РНП-частицы, по-видимому, содержат мРНК. РНП-частицы выделяли в растворах с двумя различными ионными силами (рис. 14.17). Одни частицы были выделены в «ооцитном» буфере, содержащем 0,35 мМ К+ и 5 мМ Mg2+, т.е. при ионных условиях, соответствующих неоплодотво-
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. 212_______________ ГЛАВА 14__________________________________________________________
ренному ооциту. Другие частицы выделяли в присутствии 0,35 мM Na +, т. е. при той концентрации ионов, когда должны удаляться белки, связанные с мРНК нековалентными связями. мРНК-содержащие частицы, полученные в «ооцитном» буфере, транслировались в бесклеточной системе очень плохо. А РНП, экстрагированные в Na-содержащем буфере, была способна поддерживать белковый синтез почти так же хорошо, как мРНК, выделенная из ооцитов. Поэтому полагают, что приток натрия при оплодотворении может дестабилизировать РНП-частицу, благодаря чему ее мРНК сможет транслироваться (Raff, 1980). Недавно маскирование запасенных мРНК удалось связать с определенными белками, специфичными для ооцитов. Ооциты содержат мРНК-связывающие белки, которые отличаются от аналогичных белков соматических клеток, и некоторые из этих специфических для ооцита мРНК-связывающих белков узнают определенные последовательности (Audet et al., 1987). Эти различия могут иметь важное функциональное значение. Если глобиновую мРНК инъецировать в ооциты Xenopus, то она будет эффективно транслироваться. Однако если эту мРНК предварительно смешать с белками, выделенными из РНП-частиц ооцитов шпорцевой лягушки, то наблюдается крайне незначительный уровень трансляции. РНК-связывающие белки, выделенные из других тканей, не влияли на трансляционную способность инъецированных глобиновых мРНК. Следовательно, специфические для ооцита белки РНП-частиц участвуют в трансляционной регуляции запасенных материнских мРНК (Richter, Smith. 1984). Известно, что в неоплодотворенном ооците морского ежа в составе полисом содержится менее 1% рибосом, тогда как в бластомерах на стадии дробления в полисомы связано уже около 20% рибосом (рис. 14.18). Поскольку в это время новые мРНК не синтезируются, в полисомы, очевидно, вовлекаются предсуществующие мРНК. В трех проведенных сравнительно недавно экспериментах показано, что в полисомы у зародышей включается мРНК из РНП ооцитов. У морского ежа радиоактивно меченная РНК, которая исходно была в составе РНП ооцита, позже становится связанной с полисомами бластомеров (Young, Raff, 1979). Аналогичная закономерность наблюдалась в ходе раннего развития двустворчатых моллюсков. В этом случае при анализе свободной от белков мРНК ооцитов и зародышей в бесклеточных системах трансляции было обнаружено, что обе эти фракции кодируют одинаковые белки (Rosenthal et al., 1980). Другими словами, ооциты и зародыши содержат одинаковые наборы мРНК. Однако в полисомах ооцитов и зародышей все же имеются различаю-
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. __________________ ТРАНСЛЯЦИОННАЯ И ПОСТТРАНСЛЯЦИОННАЯ РЕГУЛЯЦИЯ РАЗВИТИЯ____________________ 213
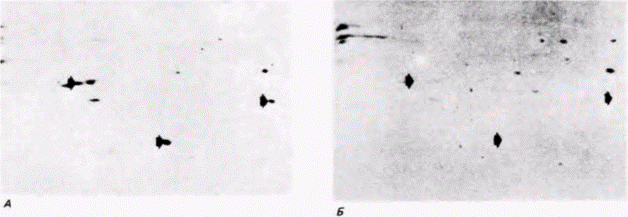
шиеся фракции мРНК. Молекулы мРНК для трех известных белков, специфичных для зародышей (А, В и С), в цитоплазме ооцита обнаруживаются в составе нетранслируемых РНК, тогда как в бластомерах зародыша они обнаруживаются в полисомной мРНК Напротив, молекулы мРНК для трех белков, характерных для ооцитов (Χ, Y и Z), выявляются в полисомах ооцитов, но не зародышей. Таким образом, можно проследить рекрутирование мРНК из нетранслируемых РНП в транскрипционно активные полисомы. Рекрутирование мРНК наблюдается также у зародышей Drosophila. Из РНП и полисом ооцита, а также полисом зародышей дрозофилы выделили поли(А)-содержащую мРНК, которую затем транслировали в бесклеточной системе, содержащей радиоактивные аминокислоты (Mermod et al., 1980). Было обнаружено, что на мРНК из РНП ооцитов можно синтезировать определенные белки, которые нельзя синтезировать на мРНК из полисом ооцитов (рис. 14.19, А, Б). Однако эти белки можно синтезировать на мРНК, выделенной из полисом зародыша (рис. 14.19.0). Следовательно, мРНК, первоначально запасенная в РНП-частицах ооцита, вовлекается в полисомы зародыша. Таким способом инициация трансляции контролирует экспрессию генов. мРНК БЕЗ КЭП-ГРУППЫ. Для эффективной трансляции необходимы 5'- и 3'-концы мРНК. Мы уже видели, как различия в длине 3’-поли(А)-хвостов
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. 214_______________ ГЛАВА 14____________________________________________________________________________
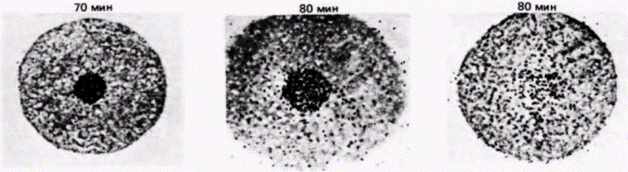
могут влиять на дифференциальную трансляцию РНК в ооцитах Spisula. Некоторые бабочки используют для трансляционного контроля механизм, связанный с изменениями 5'-кэп-группы (Kastern et al., 1982). Чтобы эффективно транслироваться, почти все эукариотические мРНК нуждаются в присутствии на своих 5'-концах кэп-группы, содержащей 7-метилгуанозин (Shatkin, 1976). В ооците табачного бражника запасенные мРНК имеют неметилированную кэп-группу, при этом гуанозин содержится, но к нему не добавлена метильная группа. Такие мРНК не транслируются в белки в бесклеточной системе. Однако при оплодотворении в ооцитах бражника проходит волна метилирования и завершается формирование кэп-групп. Молекулы мРНК, обладающие сформированными кэп-группами, способны затем связаться с рибосомами и инициировать трансляцию. В любом случае, замаскирована ли молекула мРНК белками или не завершена модификация ее 5’-конца, инициация трансляции будет подавлена. Эта молекула может не транслироваться до тех пор. пока не поступит соответствующий сигнал. КОМПАРТМЕНТАЛИЗОВАННЫЕ мРНК. В некоторых работах подвергается сомнению вывод о том, что ооцитные РНП не способны к трансляции. Вместо этого полагают, что белоксинтезирующий аппарат в ооците компартментализован, благодаря чему закрыт доступ мРНК (в составе РНП) к рибосомам (Moon et al., 1982). Синтез гистоновых мРНК в ооцитах морского ежа регулируется, по-видимому, с помощью разграничения такого типа. Гистоновые мРНК локализованы не в цитоплазме ооцита, а в его большом пронуклеусе. И только по завершении оплодотворения, когда пронуклеус разрушается, гистоновая мРНК выходит в цитоплазму (рис. 14.20) (DeLeon et al., 1983). Этого может не быть в случае других мРНК. В пронуклеусе находится менее 0,1% всей мРНК ооцита (Angerer, Angerer, 1981), а те РНП, которые содержат мРНК для актина и тубулина, локализованы преимущественно в цитоплазме (Showman et al., 1982). Известно, что некоторые материнские мРНК, как и отдельные рибосомы, присоединены к цитоскелету (Moon et al., 1983), следовательно, цитоскелет также может отделить молекулы мРНК от рибосом. ИЗМЕНЕНИЕ ЭФФЕКТИВНОСТИ ТРАНСЛЯЦИИ. В предложенных ранее моделях трансляционной регуляции предполагается, что транскрипционный аппарат способен эффективно транслировать любую мРНК, но что мРНК и рибосомы физически или химически отделены друг от друга. На самом деле этого не требуется. Исходно низкое значение pH в ооците само по себе может препятствовать синтезу белка. Как обсуждалось в гл. 2, у морского ежа в ходе оплодотворения происходит значительное высвобождение ионов водорода, приводящее к увеличению значения pH в цитоплазме с 6,9 до 7,4. Из неоплодотворенных ооцитов морского ежа группой исследователей была получена бесклеточная систе-
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. __________ ТРАНСЛЯЦИОННАЯ И ПОСТТРАНСЛЯЦИОННАЯ РЕГУЛЯЦИЯ РАЗВИТИЯ_________________ 215
ма трансляции in vitro (Winkler, Steinhardt, 1981). Значение pH в полученной суспензии либо сохраняли неизменным, либо изменяли с помощью диализа и затем измеряли включение радиоактивного валина в белки. Экзогенную мРНК не добавляли. На рис. 14.21 показаны результаты одного из таких экспериментов. Увеличение значения pH с уровня ооцита (pH 6,9) до уровня зиготы (pH 7.4) вызывало подъем белкового синтеза, напоминающий тот, что происходит при оплодотворении. Было высказано предположение, что изменение pH активирует трансляционный аппарат яйца (Hille et al., 1985; Danilchik et al., 1986). Рибосомы и факторы инициации, выделенные из ооцитов, были менее активны при трансляции, чем рибосомы, полученные из оплодотворенных яиц. Кроме того, инъекция экзогенной глобиновой мРНК в неоплодотворенные яйцеклетки не увеличивала количества синтезируемого белка. Глобиновая мРНК транслировалась за счет других мРНК, что свидетельствует о наличии какого-то компонента трансляционного аппарата в лимитирующем количестве. Лимитирующим фактором является, вероятно, фактор инициации трансляции. Добавление эФИ-2В (ГТФ-связывающий фактор циклов) или эФИ-4F (кэп-связывающий белок) к лизату, приготовленному из неоплодотворенных яйцеклеток, приводило к увеличению трансляционной эффективности этого лизата (Colin et al., 1987; Lopo et al., 1988). Вполне вероятно, что подщелачивание цитоплазмы яйца служит как для демаскирования мРНК, так и для активации факторов инициации. Это положение получило подтверждение в опытах, показавших трехкратное увеличение связывания мРНК с рибосомами после повышения значения pH (Winkler et al., 1985). При этом не наблюдалось присоединения ооцитных мРНП к рибосомам. Следовательно, яйцеклетка морского ежа регулирует трансляцию как путем изменения доступности мРНК, так и путем активации факторов инициации трансляции. Существует много способов регуляции трансляции запасенных в яйцеклетке мРНК, и различные организмы могут использовать несколько таких способов одновременно. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|