|
|
СОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДААроматическими называют углеводороды, содержащие бензольное ядро. В 1925 г. М. Фарадей выделил из состава конденсированных остатков светильного газа, который оказался тождественным веществу, полученному Э.Митчерлихом в 1834 г. перегонкой бензойной кислоты, элементный состав которого был установлен как С6Н6, получивший название бензин. Позже Ю. Либих предложил назвать это соединение бензолом. На основании экспериментальных данных для ароматических соединений выявляют следующие свойства: · реакции замещения; · устойчивость к реакциям окисления; · высокая термическая устойчивость. Первая попытка объяснения таких свойств бензола была предпринята в 1865 г. Ф. Кекуле, который сделал предположение, что двойные связи не фиксированы и происходит их быстрое перемещение (осцилляция).
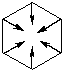
Наряду с формулой Ф. Кекуле были предложены и другие формулы бензола:
По данным рентгеноструктурного анализа, молекула бензола является плоским правильным шестиугольником с длинами связей С–С и С–Н, соответственно 0,139 нм и 0, 109 нм.
Таким образом, наиболее близкими к этим данным были формулы Кекуле и Тиле. Cтруктурные изомеры бензола, такие как, бицикло[2,2,0]гек-садиен-2,5 (бензол Дьюара, Ван-Гамен 1963 г.), призман (бензол Ландебурга – Вийе, 1964 г.), бензвален, были получены при фотохими-ческих реакциях. Все они имеют неплоское строение и оказались малостабильными, легко переходят друг в друга и в бензол при нагревании или облучении:
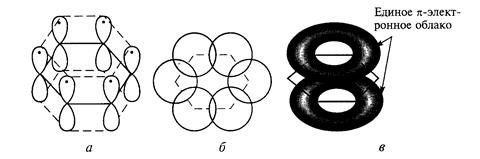
В 1889 г. Тиле выдвинул теорию "парциальных валентностей", согласно которой в сопряженных органических соединениях в области простых связей существует частичная двоесвязанность за счет остаточных "парциальных валентностей", природа которых неизвестна. Атом углерода вsp2гибридизации имеет по одной негибридизованной орбитали, расположенной перпендикулярно плоскости σ-связей (рис. 22, а). При этом каждая р-АО перекрывается в равной степени с двумя соседними (рис. 22, б). В составе общего облака р-электроны не локализованы возле своих углеродных атомов, а перемещаются свободно по единой π-молекулярной орбитали (рис. 22, в). Образование единого молекулярного облака можно рассматривать как результат эффекта π,π-сопряжения трех π-связей в молекуле бензола. Эффект сопряжения в молекуле бензола объясняет все особенности его строения и химических свойств. Благодаря максимально выраженному эффекту сопряжения образующееся общее π-электронное облако абсолютно симметрично, поэтому все связи С–С в цикле выравниваются. π-Электроны в составе общего облака получают большую степень свободы, что делает молекулу более устойчивой.
Рисунок 22 – Строение бензола
Реакции присоединения затруднены у бензола по той причине, что продуктами реакции должны были бы являться неароматические молекулы с более высокой энергией. По той же причине (высокая термодинамическая устойчивость) бензол не подвергается действию окислителей в обычных условиях. Исследования показали, что не любой циклический углеводород с чередующимися двойными и одинарными связями обнаруживает признаки ароматичности. Возникновение ароматичности связано с вполне определенным числом π-электронов в системе сопряжения. Ароматичность. Это аномально низкая энергия невозбужденного состояния, вызванная делокализацией π-электронов. Э.Хюккель (1931 г.) сформулировал условия, при которых можно прогнозировать проявление ароматичности: повышенной термодинамической стабильностью могут обладать такие циклические системы, которые имеют плоское строение и содержат в замкнутой системе сопряжения 4n+2 электронов, где n – целое число. Классификация ароматических соединений.Арены подразделяются в зависимости от: · числа циклов; · способа соединения циклов. Самыми простыми являются моноарены. Полициклические подраз-деляются на арены с: · изолированными циклами; · конденсированными циклами. Существуют три основных типа конденсированных систем: · линейно конденсированные циклы; · ангуллярно конденсированные циклы; · периконденсированные циклы.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|