
|
|
Методика и порядок измеренийЛабораторная работа № 2.2
РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА
Ознакомьтесь с теорией в конспекте и учебниках. Запустите программу «Открытая физика 1.1». Выберите раздел «Термодинамика и молекулярная физика» и работу «Распределение Максвелла». Нажмите кнопку с изображением страницы во внутреннем окне. Прочитайте теорию и запишите необходимое в свой конспект лабораторной работы. Закройте окно теории, нажав кнопку с крестом в правом верхнем углу внутреннего окна.
Цели работы: * Знакомство с компьютерной моделью, описывающей поведение молекул идеального газа. * Экспериментальное подтверждение распределения Максвелла молекул идеального газа по скоростям. * Экспериментальное определение массы молекул в данной модели. Краткая теория
Вероятностью Рi получения некоторого результата измерения называется предел отношения количества измерений, давших этот результат (Ni), к полному числу измерений N, когда N ® ¥. Элементарной вероятностью dPu при измерении величины скорости u называется вероятность наличия скорости величиной от u до u + du. Эта вероятность пропорциональна приращению скорости du: dPu = F(u) du, где коэффициент пропорциональности F(u) называется функцией распределения молекул по величине скорости. Она может быть выражена через другие функции распределения F(u) = j(uX)×j( uY)×j( uZ)×4pu2 = f(u)×4pu 2, где j(uX), ×j(uY) и×j(uZ) - функции распределения для соответствующих проекций скоростей молекул, а f(u) - их произведение. Предполагая, что газ состоит из очень большого числа N тождественных молекул, находящихся в состоянии беспорядочного теплового движения при одинаковой температуре, что силовое поле на газ не действует и, применяя методы теории вероятностей, Максвелл нашел функцию F(u):
Средняя скорость
средняя квадратичная скорость
Наивероятнейшей называется скорость u ВЕР, при которой F(u) имеет максимум:
Методика и порядок измерений
Внимательно рассмотрите рисунок 2.2.1 и зарисуйте необходимое в свой конспект лабораторной работы. Внимательно рассмотрите изображение на экране монитора компьютера. Обратите внимание на систему частиц, движущихся в замкнутом объеме слева во внутреннем окне. Они абсолютно упруго сталкиваются друг с другом и со стенками сосуда. Их количество около N = 100 и данная система является хорошей «механической» моделью идеального газа. В процессе исследований можно останавливать движение всех молекул (при нажатии кнопки « çê» вверху) и получать как бы «мгновенные фотографии», на которых выделяются более ярким свечением частицы (точки), скорости которых лежат в заданном диапазоне Du вблизи заданной скорости u (т.е. имеющие скорости от u до u+Du). Для продолжения наблюдения движения частиц надо нажать кнопку «uu». Запишите в тетрадь значение Du, указанное на экране.
Рис. 2.2.1. Окно опыта Измерения 1. Нажмите кнопки «uu», «Старт» и «Выбор» и установите температуру Т1 , указанную в табл. 2.2.1 для вашей бригады. Запишите для нее значение наивероятнейшей скорости. 2. Установите скорость выделенной группы молекул вблизи минимального заданного в табл. 2.2.2 значения. 3. Нажмите клавишу « çê» и подсчитайте на «мгновенной фотографии» количество молекул DN, скорости которых лежат в заданном диапазоне Du вблизи заданной скорости молекул u (они более яркие). Результат запишите в табл. 2.2.2. 4. Нажмите кнопку «uu» и через 10-20 секунд получите еще одну мгновенную фотографию (нажав кнопку « çê»). Подсчитайте количество частиц с заданной скоростью. Результат запишите в табл.2.2.2. 5. Повторите еще 3 раза измерения для данной скорости и результаты запишите в табл.2.2.2. 6. Измените скорость до значения, указанного в табл.2.2.2., и сделайте по 5 измерений (как в пункте 4) для каждой скорости. Вблизи максимума функции распределения шаг при изменении скорости делать равным Du = 0.1 км/с. 7. Установите (как в пункте 1) вторую температуру Т2 из табл.2.2.1. Запишите для нее значение наивероятнейшей скорости. 8. Повторите измерения (по пунктам 2,3,4,5), записывая результат в табл.2.2.3, аналогичную табл.2.2.2.
Таблица 2.2.1 Примерные значения температуры(не перерисовывать)
Таблицы 2.2.2, 2.2.3 Результаты измерений при T = ____ K 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2024 stydopedia.ru Все материалы защищены законодательством РФ.
|
 .
. ,
, .
.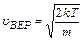 .
.